作者:石油醚
导读:
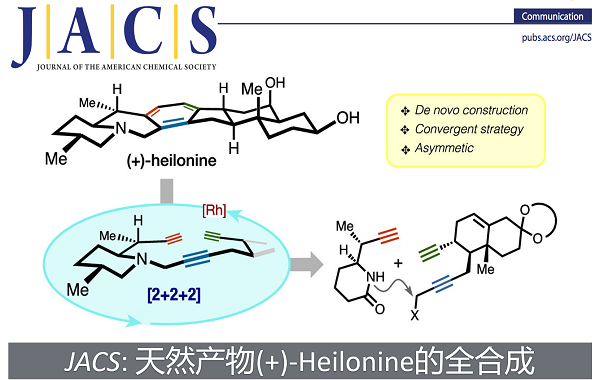
近日,芝加哥大学的Viresh H. Rawal教授团队在J. Am. Chem. Soc.上,以 “Enantioselective Total Synthesis of (+)-Heilonine”为题,以21步首次完成了(+)-Heilonine的全合成。其中,关键步骤主要涉及: Rh催化的[2+2+2]环化异构化(Rh catalyzed [2 + 2 + 2] cycloisomerization reaction); 不对称Diels–Alder反应 (asymmetric Diels–Alder reaction ); Robinson环化 (Robinson annulation)等。
“Enantioselective Total Synthesis of (+)-Heilonine
Kyle J. Cassaidy and Viresh H. Rawal*
J. Am. Chem. Soc., 2021, 143, 16394–16400. doi: 10.1021/jacs.1c08756”
正文:
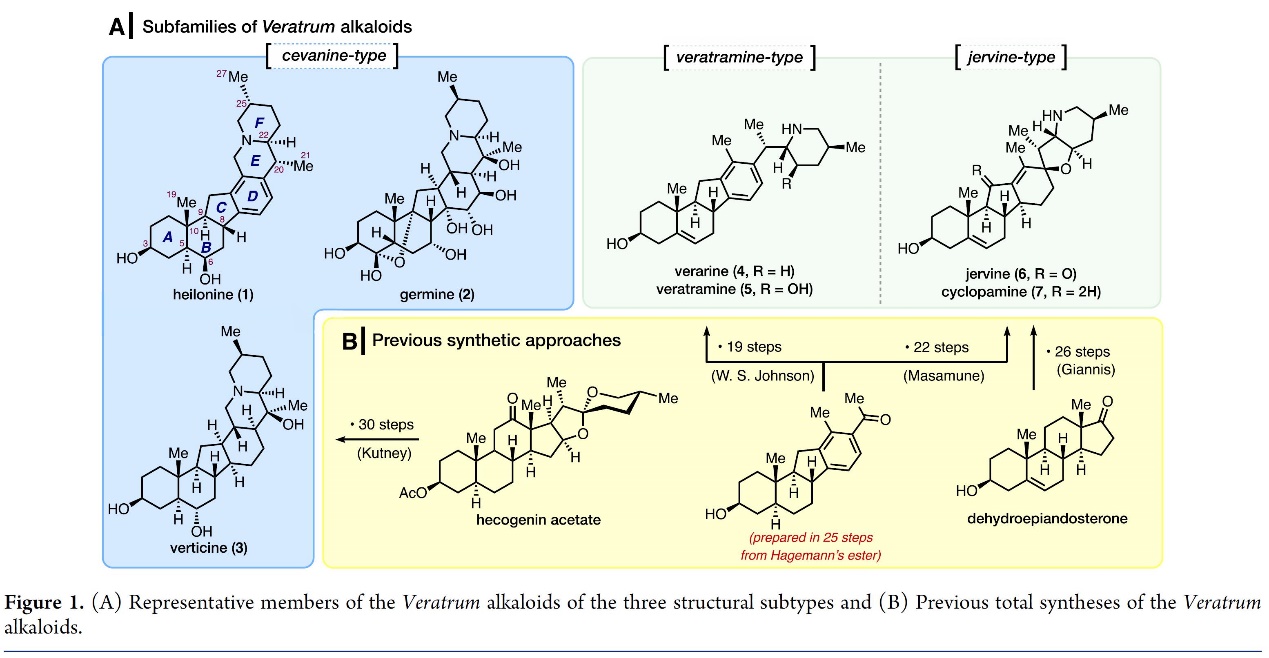
甾体生物碱因其独特的骨架和特殊的生物活性引起了众多科学家广泛的关注[1]。从百合科藜芦属植物中分离得到藜芦(Veratrum)生物碱就是其中之一。从结构上看,藜芦(Veratrum)生物碱具有共同的C-nor-D-homo甾体骨架,而根据其与哌啶环(F环)的连接方式可分为三类:cevanine型、veratramine型和jervine型(Figure 1)[2]。Heilonine (1)就是cevanine型生物碱,其是由日本科学家Koh Kaneko 教授及其同事于1989年从黑龙江省百合科植物平贝母Fritillaria Ussuriensis Maxim.中分离获得 (Figure 1)[3],并且其被认为是重要的中草药“贝母”的成分(传统中医中用来镇静、止咳和祛痰) [4]。此外,Koh Kaneko 教授通过通过NMR和X射线晶体学分析阐明了其具有复杂六环结构和九个立体中心。近日,Viresh H. Rawal教授团以21步首次完成了(+)-Heilonine的全合成,并发表于J. Am. Chem. Soc.上。
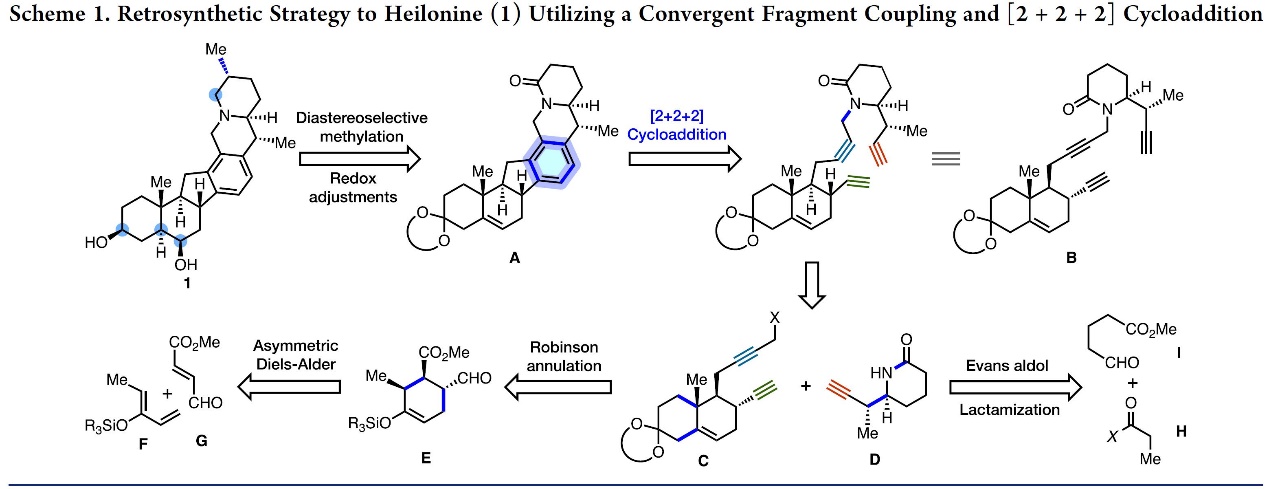
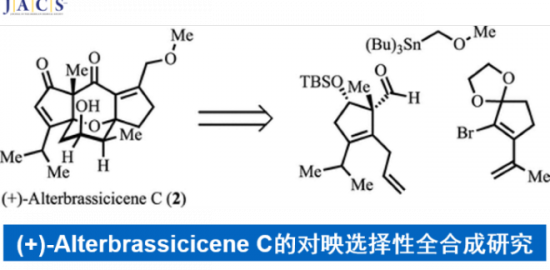
首先,(+)-Heilonine (1)具有复杂的六环结构以及9个立体中心。基于上述骨架,作者对(+)-Heilonine (1)进行了相关的逆合成分析(Scheme 1)。即以醛G和烯醇硅醚F为原料经不对称Diels-Alder环加成获得六元环E,E经Robinson环化得到砌块双环二炔C。另外一个砌块哌啶酮D可由丙酰化合物H和醛经不对称Evans aldol反应以及 lactamization(引入N)合成。双环二炔C和哌啶酮D为原料经烷基化反应得中间体B,B通过Rh催化的[2+2+2]环化异构化合成关键砌块A[5]。最后,关键中间体A通过非对映选择性甲基化和氧化反应完成(1)的全合成。
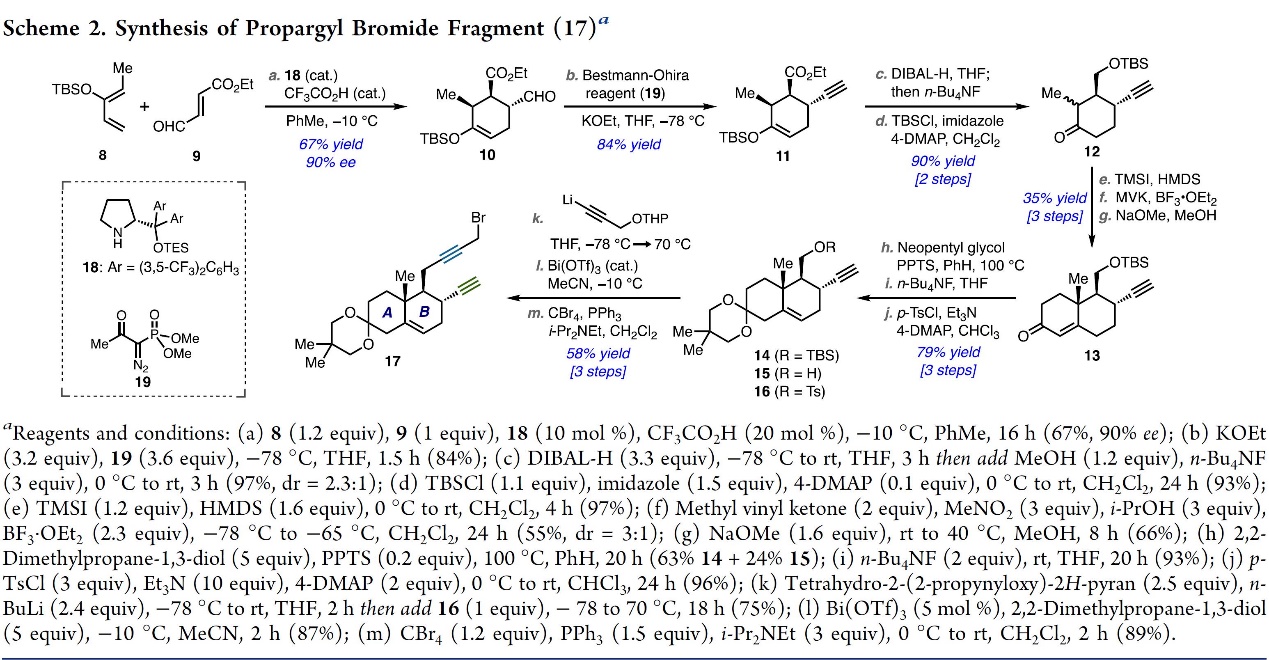
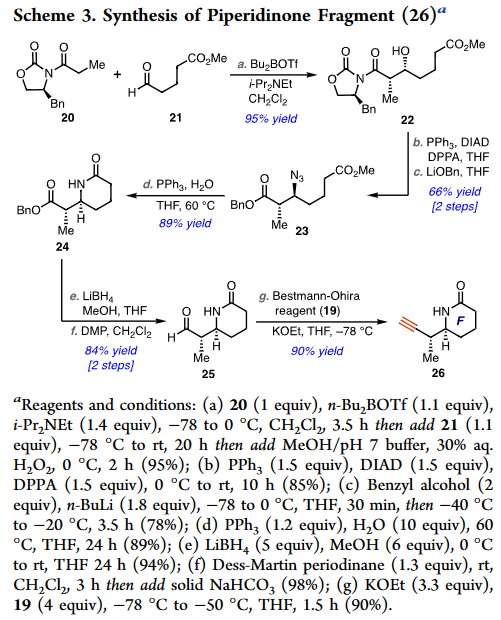
首先,该小组合成了砌块17和26,如Scheme 2, 3。


该小组完成了Vilmoraconitine (3)的合成路线设计,如Scheme 4。
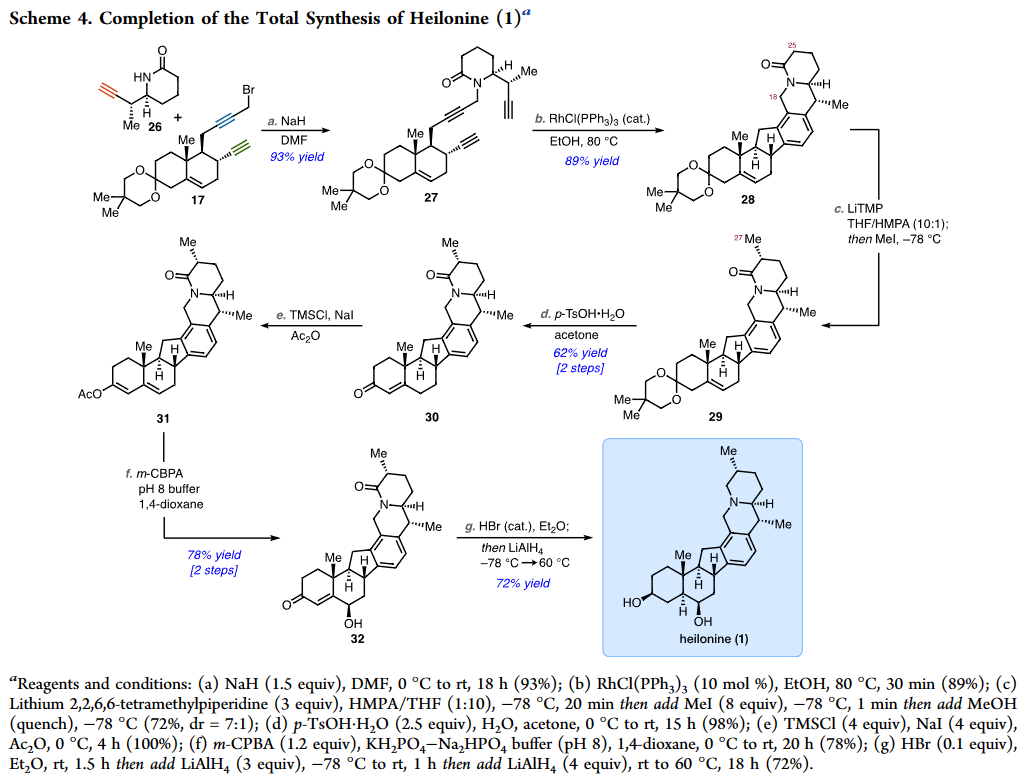

总结,芝加哥大学的Viresh H. Rawal教授团队以21步首次完成了(+)-Heilonine的全合成。其中,关键步骤主要涉及: Rh催化的[2+2+2]环化异构化(Rh catalyzed [2 + 2 + 2] cycloisomerization reaction); 不对称Diels–Alder反应 (asymmetric Diels–Alder raection ); Robinson环化 (Robinson annulation)等
参考文献:
- [1] Q.-W. Jiang, M.-W. Chen, K.-J. Cheng, P.-Z. Yu, X. Wei, Z. Shi, Med. Res. Rev. 2016, 36, 119. doi: 10.1002/med.21346.
- [2] H.-J. Li, Y. Jiang, P. Li, Nat. Prod. Rep. 2006, 23, 735. doi: 10.1039/B609306J.
- [3] Y. Kitamura, M. Nishizawa, K. Kaneko, M. Shiro, Y.-P. Chen, H.-Y. Hsu, Tetrahedron 1989, 45, 7281. doi: 10.1016/S0040-4020(01)89188-2.
- [4] X. Wu, S.-w. Chan, J. Ma, P. Li, P.-c. Shaw, G. Lin, J. Ethnopharmacol. 2018, 210, 39. doi: 10.1016/j.jep.2017.08.027.
- [5] S. Saito, Y. Yamamoto, Chem. Rev. 2000, 100, 2901. doi: 10.1021/cr990281x.
- [6] S. Müller, B. Liepold, G. J. Roth, H. J. Bestmann, Synlett 1996, 1996, 521. doi: 10.1055/s-1996-5474.
- [7] P. Duhamel, G. Dujardin, L. Hennequin, J.-M. Poirier, J. Chem. Soc., Perkin Trans. 1 1992, 387. doi: 10.1039/P19920000387.
- [8] Y. Yamamoto, T. Arakawa, R. Ogawa, K. Itoh, J. Am. Chem. Soc. 2003, 125, 12143. doi: 10.1021/ja0358697.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.


















No comments yet.