本文作者:杉杉
导读
近日,Yale大学的J. A. Ellman团队在Angew. Chem. Int. Ed.中发表论文,首次报道一种全新的采用Co(III)催化剂促进的1,3-烯炔与醛之间的立体选择性串联C-H键加成反应方法学,进而成功完成一系列联烯醇 (allenyl alcohol)分子的构建。
Stereoselective Synthesis of Allenyl Alcohols by Cobalt(III)-Catalyzed Sequential C−H Bond Addition to 1,3-Enynes and Aldehydes
Xu, J. P. Tassone, B. Q. Mercado, J. A. Ellman, Angew. Chem. Int. Ed. 2022, ASAP. doi: 10.1002/anie.202202364.
正文
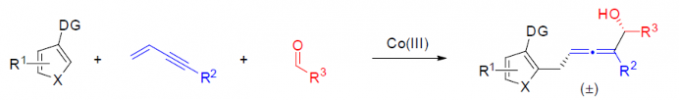
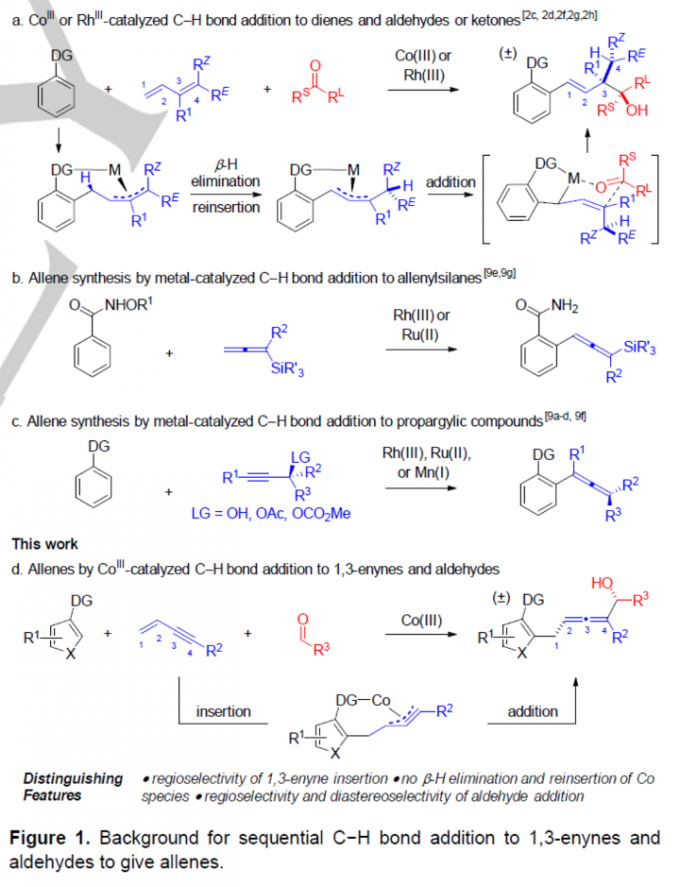
近年来,串联C-H键加成反应方法学的相关研究已经备受有机合成化学家的广泛关注 (Figure 1a-c)[1]-[8]。然而,通过1,3-烯炔的C-H键加成策略实现联烯分子构建的合成转化方法学研究,目前却尚未有相关的文献报道。这里,Yale大学的J. A. Ellman课题组成功设计出首例通过Co(III)催化剂促进的1,3-烯炔与醛之间的立体选择性串联C-H键加成反应方法学 (Figure 1d)。
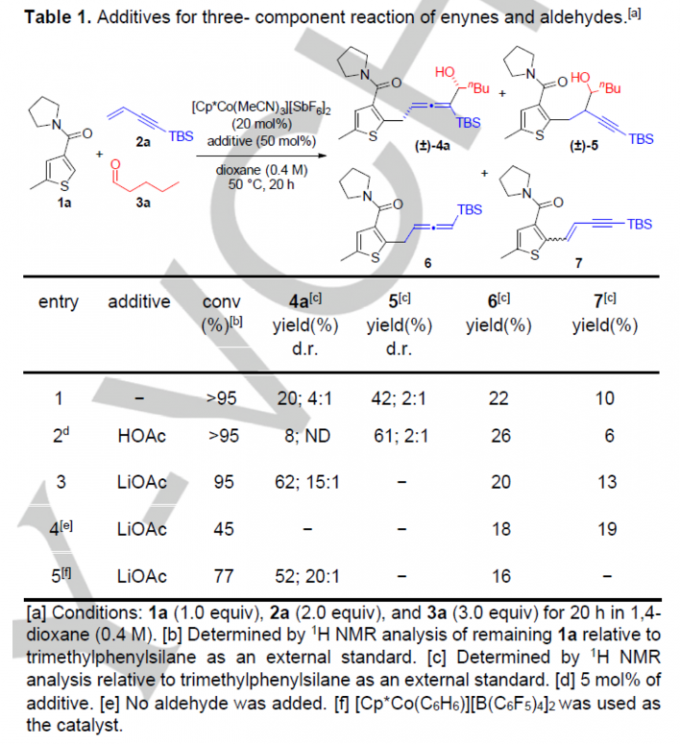
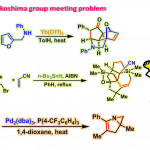
首先,作者采用1a、1,3-烯炔衍生物2a与戊醛3a作为模型底物,进行相关
反应条件的优化筛选(Table 1)。进而确定最佳的反应条件为:采用[Cp*Co(MeCN)3][SbF6]2作为催化剂,LiOAc作为添加剂,1,4-二氧六环作为反应溶剂中,反应温度为50oC,最终获得62%收率的三组分反应产物4a (dr为15:1)。
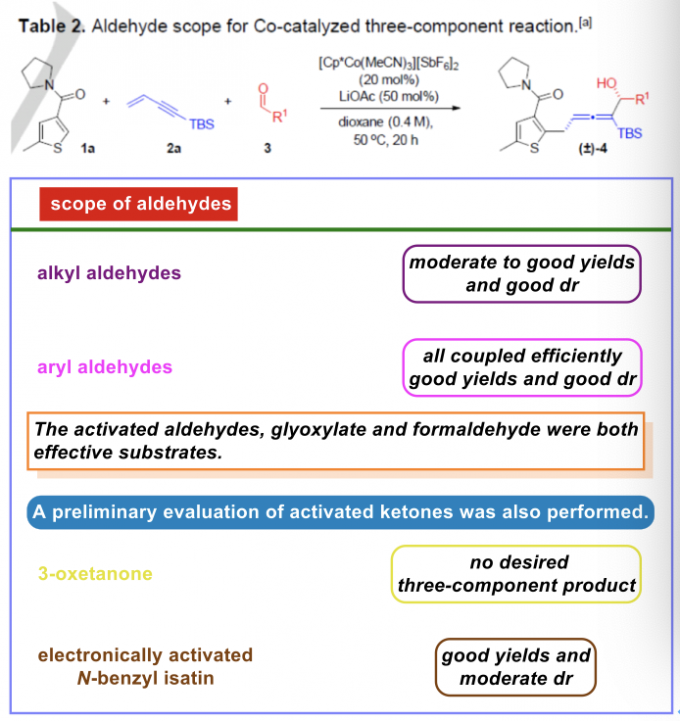
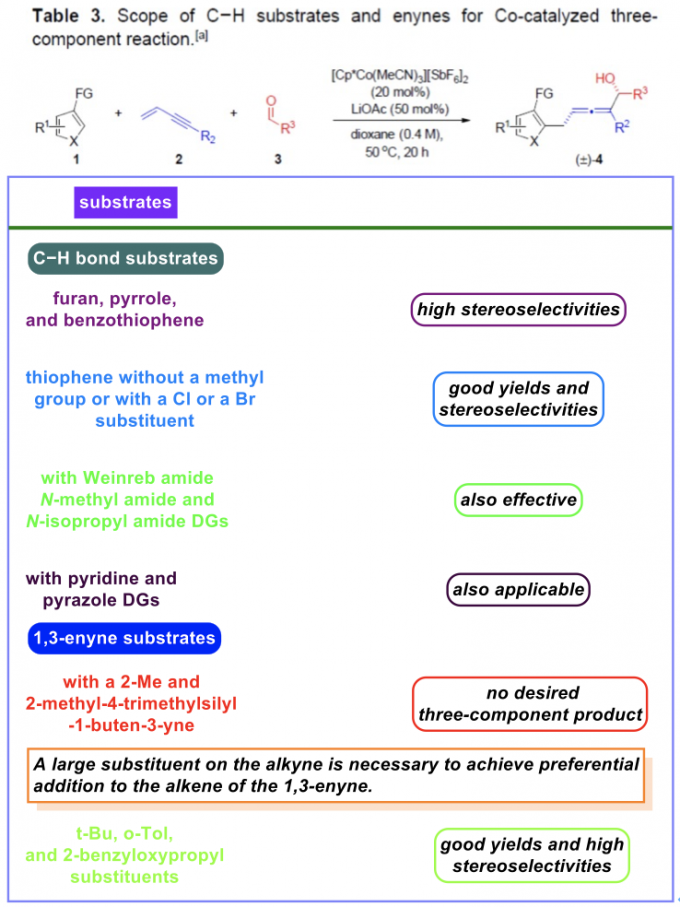
在上述的最佳反应条件下,作者分别对一系列醛 (Table 2) 与各类具有C-H键的有机底物以及烯炔底物 (Table 3)的应用范围进行深入研究。
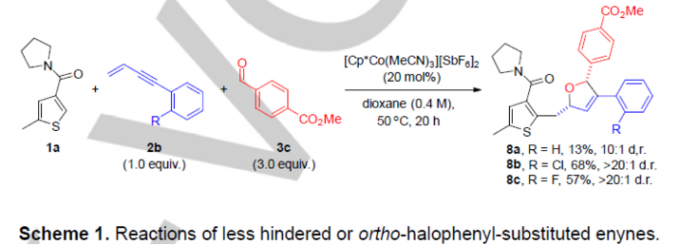
同时,该小组进一步对炔基末端带有苯基或邻卤代苯基取代的烯炔底物进行进一步研究 (Scheme 1),进而高度立体选择性地完成相应二氢呋喃分子的构建。
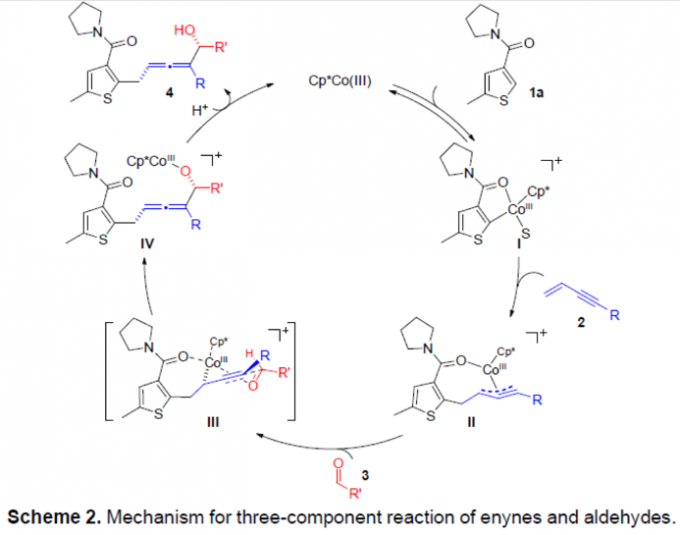
基于前期的文献报道[9],作者提出如下合理的反应机理 (Scheme 2)。
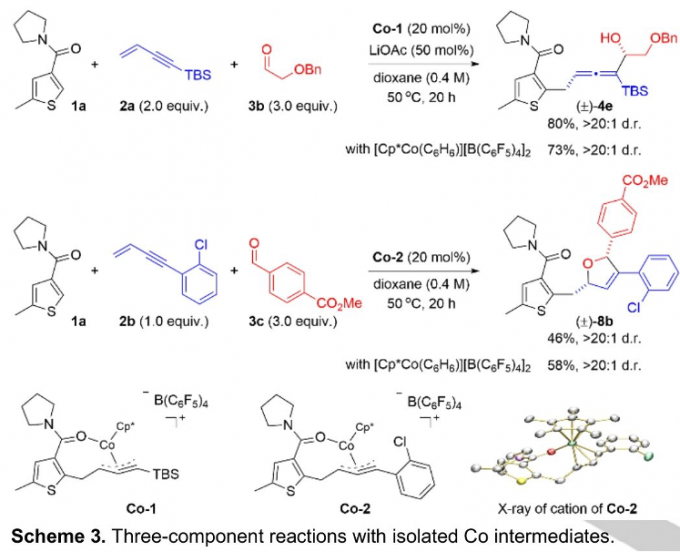
同时,该小组进一步通过原位制备并分离出的Co-1与Co-2中间体 (Scheme 3)参与的三组分反应过程,进而进一步支持上述的反应机理路径。
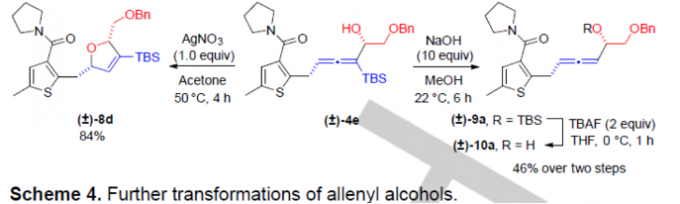
之后,该小组进一步通过如下的一系列研究表明,这一全新的串联C-H键加成反应策略具有潜在的合成应用价值 (Scheme 4)。
总结
Yale大学的J. A. Ellman课题组成功设计出首例采用Co(III)催化剂促进的1,3-烯炔与醛之间的立体选择性串联C-H键加成反应方法学,进而成功完成一系列联烯醇分子的构建。这一全新的合成转化策略具有广泛的底物应用范围、优良的立体选择性以及优良的官能团兼容性等优势
参考文献
- [1] (a) R. Mi, X. Zhang, J. Wang, H. Chen, Y. Lan, F. Wang, X. Li, ACS Catal. 2021, 11, 6692. doi:10.1021/acscatal.1c01615.
- (b) D. Sun, J. A. Ellman, Angew. Chem. Int. Ed. 2021, 60, 2135. doi: 10.1002/anie.202010735.
- [2] (a) A. G. Herraiz, N. Cramer, ACS Catal. 2021, 11, 11938. doi: 10.1021/acscatal.1c03153.
- (b) M. Tang, Y. Li, S. Han, L. Liu, L. Ackermann, J. Li, Eur. J. Org. Chem. 2019, 4, 660. doi: 10.1002/ejoc.201801535.
- [3] J. A. Boerth, J. A. Ellman, Angew. Chem. Int. Ed. 2017, 56, 9976. doi: 10.1002/anie.201705817.
- [4] (a) D. S. Brandes, A. D. Muma, J. A. Ellman, Org. Lett. 2021, 23, 9597. doi: 10.1021/acs.orglett.1c03807.
- (b) D. S. Brandes, A. Sirvent, B. Q. Mercado, J. A. Ellman, Org. Lett. 2021, 23, 2836. doi: 10.1021/acs.orglett.1c00851.
- [5] T. Pinkert, M. Das, M. L. Schrader, F. Glorius, J. Am. Chem. Soc. 2021, 143, 7648. doi: 10.1021/jacs.1c03492.
- [6] (a) J. Sun, W. Yuan, R. Tian, P, Wang, X. Zhang, X. Li, Angew. Chem. Int. Ed. 2020, 59, 22706. doi:10.1002/anie.202010832.
- (b) D. Bai, J. Xia, F. Song, X. Li, B. Liu, L. Liu, G. Zheng, X. Yang, J. Sun, X. Li, Chem. Sci. 2019, 10, 3987. doi:10.1039/C9SC00545E.
- [7] (a) S. Nakanowatari, L. Ackermann, Chem. Eur. J. 2015, 21, 16246. doi: 10.1002/chem.201502785.
- (b) R. Zeng, S. Wu, C. Fu, S. Ma, J. Am. Chem. Soc. 2013, 135, 18284. doi: 10.1021/ja409861s.
- [8] (a) S. Kumar, A. M. Nair, C. M. R. Volla, Chem. Commun. 2021, 57, 6280. doi: 10.1039/C7CC90225E.
- (b) X. Wu, J. Fan, C. Fu, S. Ma, Chem. Sci. 2019, 10, 6316. doi: 10.1039/C9SC00603F.
- [9] (a) D. Sun, Z. Shen, J. A. Ellman, Angew. Chem. Int. Ed. 2019, 58, 12590. doi: 10.1002/anie.201906633.
- (b) J. A. Boerth, S. Maity, S. K. Williams, B. Q. Mercado, J. A. Ellman, Nat. Catal. 2018, 1, 673. doi: 10.1038/s41929-018-0123-4.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载




















No comments yet.