本文作者:Summer
导读
Santiago de Compostela大学 (University of Santiago de Compostela)的M. Gulías教授团队实现了基于Pd催化C-H键活化策略促进的α-支链烯丙基三氟甲磺酰胺的动力学拆分方法学,以中等程度的总反应收率与良好的对映选择性,获得一系列四氢吡啶类化合物。相关研究成果发表于
Kinetic Resolution of Allyltriflamides through a Pd-Catalyzed C−H Functionalization with Allenes: Asymmetric Assembly of Tetrahydropyridines
J. M. González, B. Cendón, J. L. Mascareñas, M. Gulías, J. Am. Chem. Soc. ASAP. doi: 10.1021/jacs.1c01929.
正文
动力学拆分 (kinetic resolutions, KR)能同时获得两种手性化合物,因而备受化学家的广泛关注。2014年,余金权团队报道了钯催化的α-支链苄胺衍生物通过C-H键碘化反应或交叉偶联反应过程而进行的动力学拆分方法学[1]。
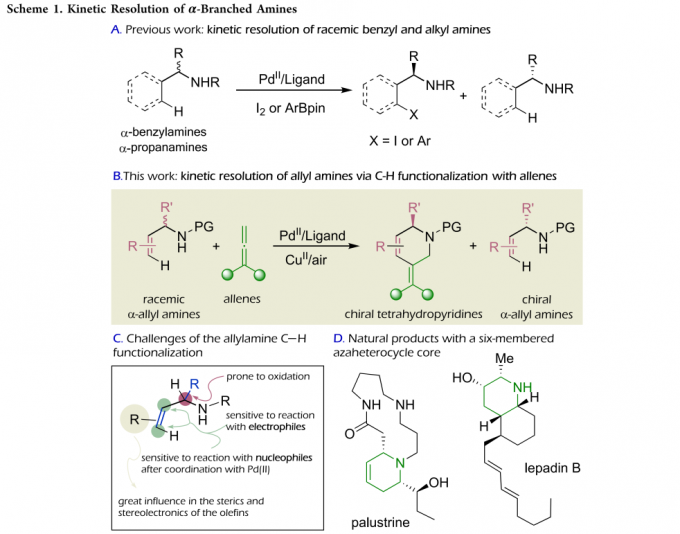
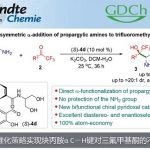
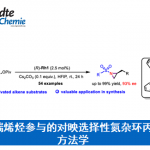
近日,Santiago de Compostela大学的M. Gulías教授团队采用Pd催化联烯C-H键活化策略,成功实现α-支链烯丙基三氟甲磺酰胺的动力学拆分方法学,并以高度的对映选择性与中等程度的反应收率,获得一系列四氢吡啶类化合物 (Scheme 1B)。而四氢吡啶类化合物则是构建一系列天然产物与生物活性化合物的关键砌块 (Scheme 1D)。
图片来源:J. Am. Chem. Soc.)
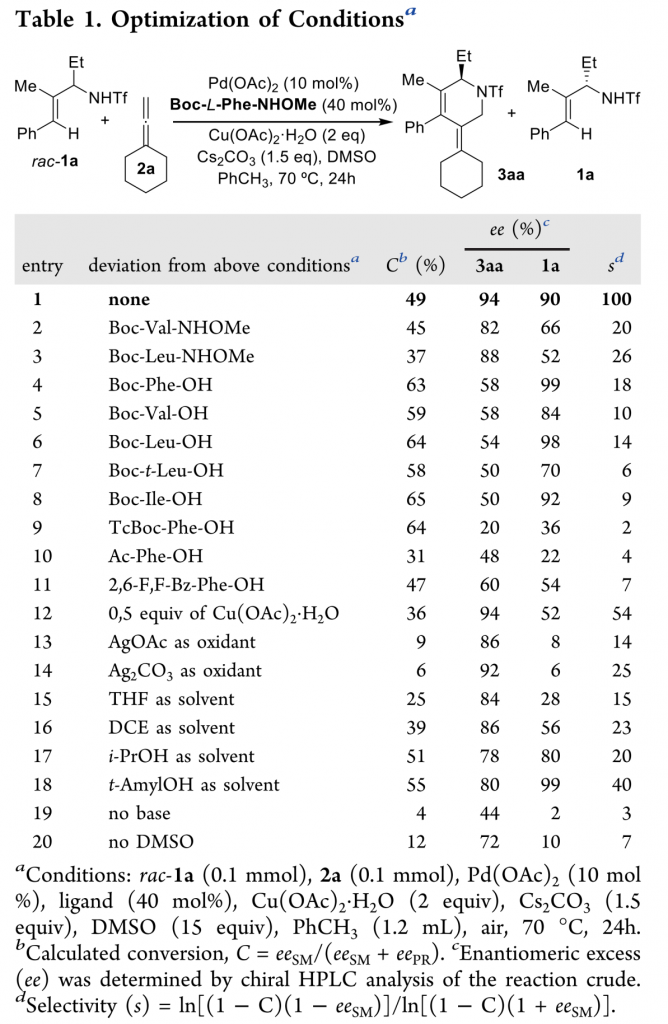
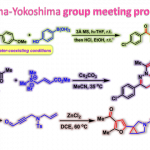
首先,作者采用外消旋的烯丙基三氟甲磺酰胺1a与联烯2a作为模板底物,通过对催化剂、添加剂以及碱等条件进行筛选,确定最佳反应条件 (Table 1)为:采用10 mol% Pd(OAc)2作为催化剂、40 mol% Boc-L-Phe-NHOMe作为配体,2.0 eq. Cs2CO3作为碱,2.0 eq. Cu(OAc)2•H2O以及15.0 eq. DMSO作为添加剂,PhCH3作为溶剂,在70 °C条件下, 反应时间为24 h,能够以46%的收率与94%的对映选择性获得手性产物3aa,并以35%的收率与90%的对映选择性回收1a中的非反应活性对映体。
(图片来源:J. Am. Chem. Soc.)
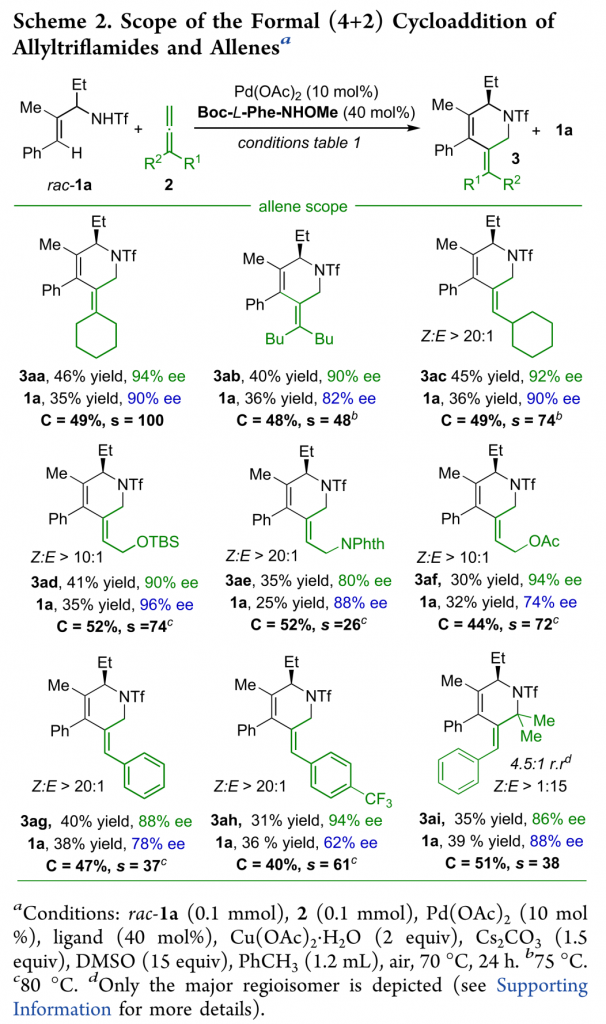
在上述最佳反应条件下,作者接下来对各类取代联烯底物的应用范围进行考察 (Scheme 2)。研究表明:适当改变反应条件,亚环己基、环己亚甲基、TBSO保护的联烯以及各类芳基取代的联烯均能较好的与上述反应条件兼容,能够以中等的收率、优良的对映选择性以及E/Z比获得相应手性产物,并以中等的收率与优秀的对映选择性回收相应的对非反应活性对映体。
(图片来源:J. Am. Chem. Soc.)
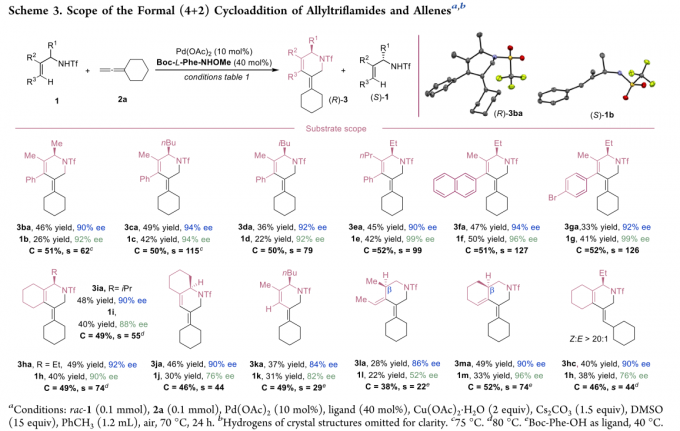
同时,作者对烯丙基三氟甲磺酰胺底物的应用范围进行考察 (Scheme 3)。研究发现,各种α-或β-具有甲基、丁基与异丁基取代的烯丙基三氟甲磺酰胺以及各类环状烯丙基三氟甲磺酰胺均能能够与上述反应条件良好的兼容,能够以中等的收率与良好的对映选择性获得相应产物及原料中的非反应活性对映体。同时,作者发现,R3为芳基取代基时,KR反应同样能够较好的进行,并以中等收率与对映选择性获得相应产物及原料中的非反应活性对映体。其中,产物3ba与1b的绝对构型均通过X射线晶体学分析确定。
(图片来源:J. Am. Chem. Soc.)
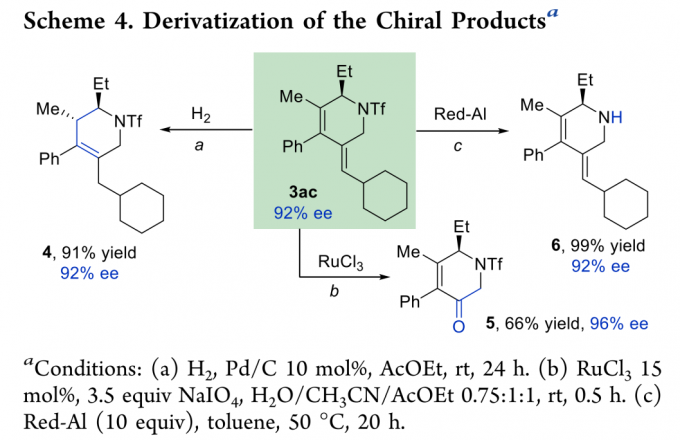
为证明该方法学的应用潜力,作者进行一系列相关的衍生反应 (Scheme 4 )。该小组观察到,在Pd/H2作用下,3ac可以还原为产物4。同时,3ac能够与RuCl3反应生成产物5。此外,作者发现,3ac中的三氟甲磺酰基能够通过Red-Al的还原而去除,生成产物6。
(图片来源:J. Am. Chem. Soc.)
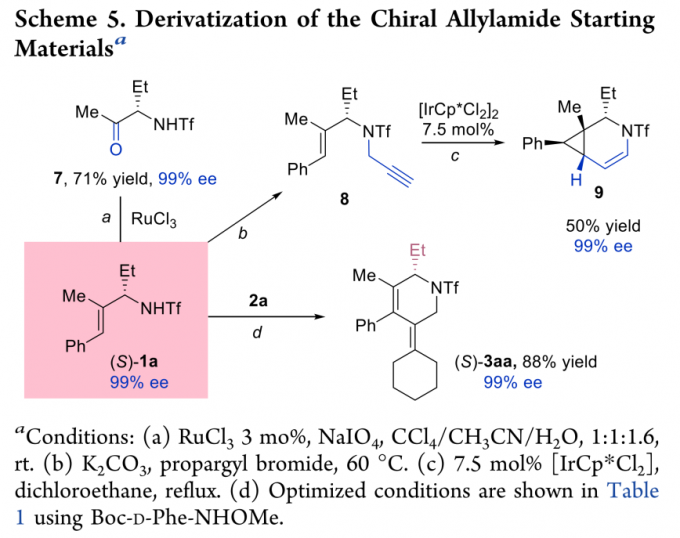
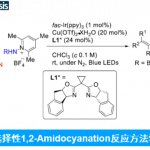
通过动力学拆分获得的起始原料的手性对映体同样可以发生各种衍生反应(Scheme 5)。例如,在氧化剂存在的条件下,(S)-1a可转化为手性氨基酮产物 (keto amino product) 7。同时,(S)-1a的NH键可以发生进一步炔基化,生成的产物8能够进一步进行环化反应,获得产物9。此外,作者发现,在最佳反应条件下,将上述Boc-L-Phe-NHOMe配体更换为相应的D-氨基酸衍生物,(S)-1a则能够与联烯2a发生[4+2]环加成反应,获得产物(S)-3aa。
(图片来源:J. Am. Chem. Soc.)
小结:Santiago de Compostela大学的M. Gulías教授团队实现了基于Pd催化C-H键活化策略进行的α-支链烯丙基胺的动力学拆分方法学,最终,以中等的收率与良好的对映选择性获得一系列四氢吡啶类化合物。
参考文献
- Chu, K. Xiao,J. Yu, Science, 2014, 346, 451. doi: 10.1126/science.1258538
- Xiao, L.Chu, G. Chen, J. Yu, J. Am. Chem. Soc. 2016, 138, 7796. doi: 10.1021/jacs.6b04660
- Xu, J. Hu, L. Wang, S. Liao, Y. Tang,J. Am. Chem. Soc. 2015, 137, 8006. doi: 10.1021/jacs.5b04429

















No comments yet.