本文作者:竹悠
导言
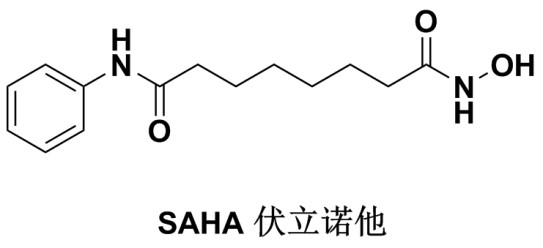
多重药理学是将多种生物活性基团组合到一个抗癌药中,各组分分别发挥作用,根据这种理念,作者设计了即含金属中心,又有抗肿瘤药物伏立诺他vorinostat(SAHA)中的2-吡啶硫代酰胺和异羟肟酸结构的有机金属药物。这些有机金属化合物可以在纳摩尔水平上抑制组蛋白去乙酰化酶histone deacetylases (HDACs)。其中有机铑Rh化合物4c是HDAC6的强效抑制剂,4c对人类肿瘤细胞具有高毒性,但溶血活性和斑马鱼毒性较低。化合物4c的药理与SAHA不同,它略微减少血管内皮生长因子受体2 (VEGFR2)的表达,说明新型的金属药物与母体结构的作用模型不同,可以开发非常规的抗肿瘤药物。
正文
组蛋白去乙酰化酶histone deacetylases (HDACs)与肿瘤的发生和转移密切相关,经常在实体瘤中过度表达,导致预后很差。HDACs与肿瘤血管再生相关,调节HDACs也可引起其他生物学活性的变化,如p53蛋白、微管蛋白tubulin、 Hsp90蛋白等。上市药物伏立诺他vorinostat(SAHA)和罗米地辛romidepsin (FK-228)都靶向HDACs中的锌离子。金属络合物的三维形状可调,这种独特的性质,在选择性识别和作用于蛋白的特定位置有关,如金属铂Pt、铼Re、铁Fe和钌Ru。
新西兰奥克兰大学University of Auckland的Muhammad Hanif等运用多重药理学的理念,像瑞士军刀一样,将SAHA的药效团和金属元素组合在一个分子中,开发了含金属元素的HDAC抑制剂,论文发表在Angew. Chem. Int. Ed上,并被选为Hot Paper。
Dr. Muhammad Hanif Dr. Jahanzaib Arshad Dr. Jonathan W. Astin Zohaib Rana Dr. Ayesha Zafar Dr. Sanam Movassaghi Dr. Euphemia Leung Kamal Patel Prof. Tilo Söhnel Dr. Jóhannes Reynisson Dr. Vijayalekshmi Sarojini Prof. Rhonda J. Rosengren Dr. Stephen M. F. Jamieson Prof. Christian G. Hartinge
A Multitargeted Approach: Organorhodium Anticancer Agent Based on Vorinostat as a Potent Histone Deacetylase Inhibitor
Angew. Chem. Int. Ed. 2020, ASAP,DOI: 10.1002/anie.202005758
1. 合成
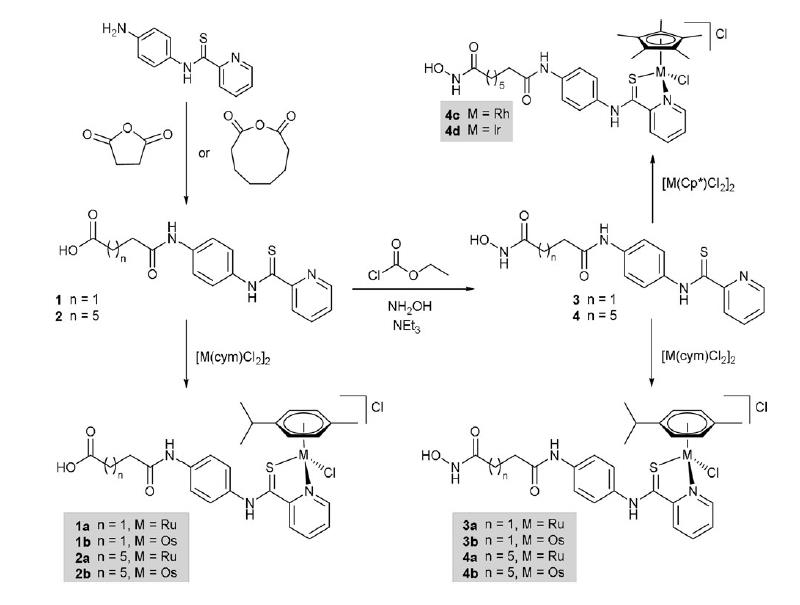
Scheme 1. 2-吡啶硫代酰胺羧酸(1和2)、异羟肟酸(3和4)及对应金属络合物的合成
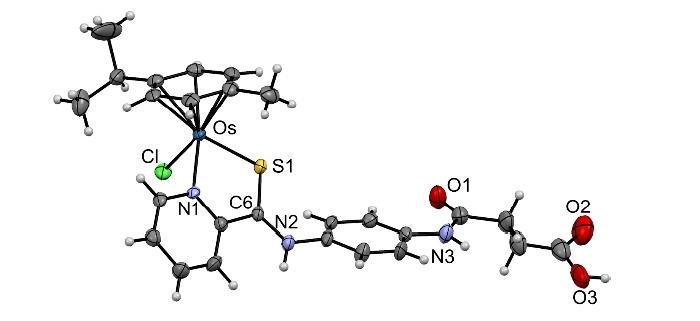
基于2-吡啶硫代酰胺PCA的化合物3和4由两步反应合成,路线如scheme 1所示。先由酸酐和胺基反应,得到羧酸1(61%)和2(41%),接着与NH2OH、氯甲酸乙酯、三乙胺等反应转化为对应的异羟肟酸3(29%)和4(32%)。再和金属二聚物前体如[M(cym)Cl2]2(M=Ru、Os)、[M(Cp*)Cl2]2(M=Rh、Ir)反应生成对应的金属有机化合物,化合物结构通过核磁、质谱确认。通过1b的单晶结构可以看到,为了与Os配位,化合物1中的N1‧‧‧HN2氢键断裂,PCA结构失去平面性,C6–S1键拉长单键属性增强,C6-N2双键属性增强,如图1所示。4a-4d在水溶液中,均发生了氯-水配体交换反应,水化产物的稳定性可保持5天。
图1. 化合物1b的单晶结构 图片来源:Angew. Chem. Int. Ed
2. 生物活性研究
2.1 细胞毒性
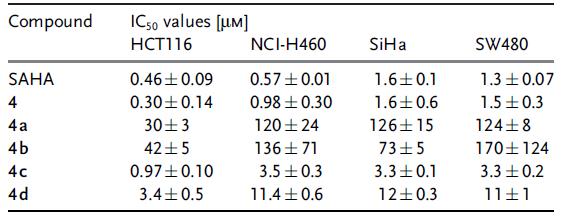
SRB(磺酰罗丹明B)实验法测定化合物1-4和对应金属络合物的对人结直肠癌human colorectal(HCT116)、非小细胞肺癌non-small cell lung (H460),宫颈癌cervical (SiHa)和结肠癌coloncarcinoma (SW480)的细胞毒性,结果见表 1。化合物4的毒性为羧酸衍生物2的2倍,说明了异羟肟酸结构是必需基团。金属络合物中Ru 4a 和Os 4b为低到中等活性,Rh 4c 和Ir 4d的活性最好,其中4c和4类似。化合物4a 和4c可以诱导活性氧ROS,但并不比对照高。
表1. 化合物4及金属络合物的体外细胞毒性
2.2 HDACs抑制性
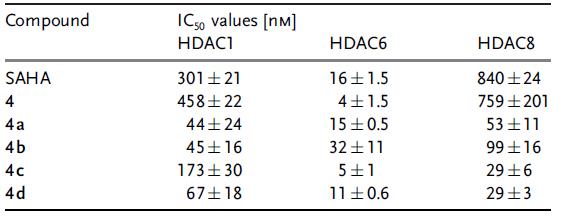
考察10μM浓度下化合物2-4和4a-4d对HDAC8的抑制性。化合物2和3的活性很差,化合物3中的异羟肟酸结构使其活性略好,也说明需要合适的脂肪碳链,使异羟肟酸结构到达锌离子的位置。所有的金属络合物活性均高于配体,因此,考察了这些金属络合物对HDAC1, HDAC6和HDAC8的抑制性。从表2可以看到,金属络合物的活性达到SAHA的10倍左右,并且表现出了对HDAC6的选择性。
表2. SAHA、化合物4及金属络合物对HDAC1、HDAC6和HDAC8的抑制性
络合物中的金属可能存在两方面原因:
1、配体交换作用,虽然没有直接证据看到与分离氨基酸的加成产物,但蛋白质微环境可以支持与HDAC中结合部位的相互作用。
2、金属部分作为一个空间较大的基团,可能形成疏水作用或氢键作用。
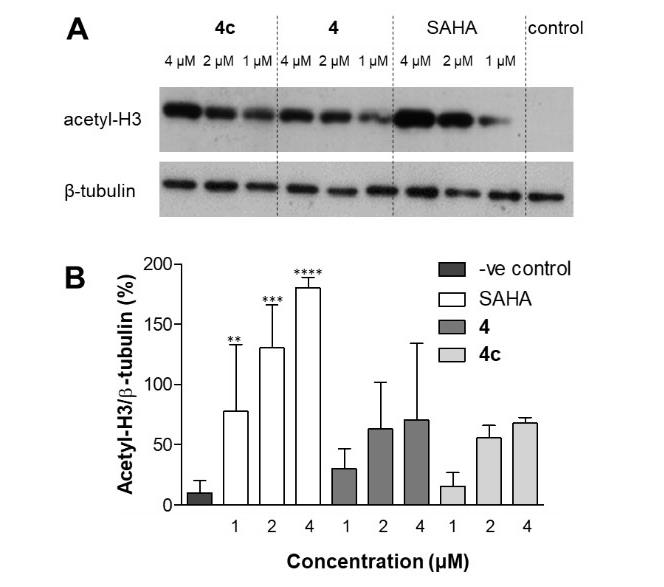
组蛋白的乙酰化和脱乙酰化,对应着转录的调控。HDACs从组蛋白上脱去乙酰基导致转录抑制,SAHA是个强效的HDAC抑制剂。在前列腺癌细胞PC3中,化合物4和4c抑制组蛋白H3脱乙酰化的效果相当,但从免疫印迹的数据看到SAHA活性要优于4和4c,如图2所示。
图2. 组蛋白变体H3对SAHA、化合物4和4c的乙酰化响应 图片来源:Angew. Chem. Int. Ed
2.3 结构和活性的关系
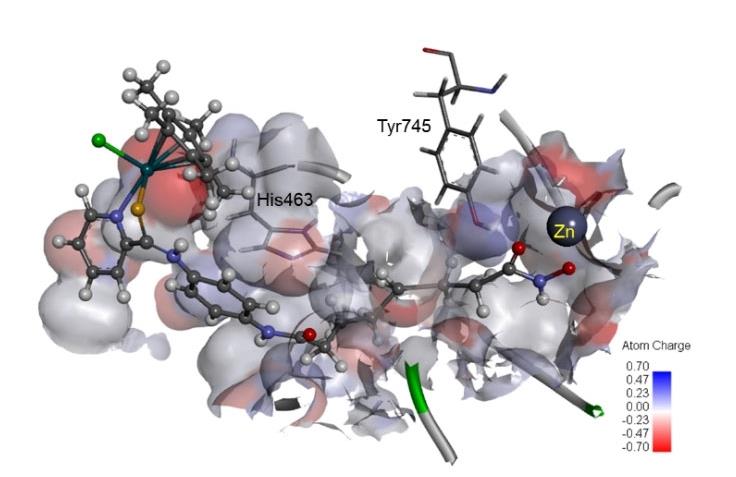
HDAC8的活性部位含有一个狭长的由疏水氨基酸构成的催化隧道口袋,4及其金属络合物恰好契合结合部位,异羟肟酸结构可以结合二价锌离子。对HDAC6,金属络合物的金属部分与蛋白的重要活性氨基酸(Tyr745、Pro464、Phe583、His463和Gly473)发生额外的作用,如图3所示。
图3. 化合物4c与HDAC6的结合 图片来源:Angew. Chem. Int. Ed
2.4 溶血研究
化合物4c对老鼠红细胞的溶血活性表明,低浓度时,无溶血活性,当增加至200μM时具有10%溶血活性,但比起顺铂100%的溶血活性,毒性还是较低的。
2.5 肿瘤血管研究
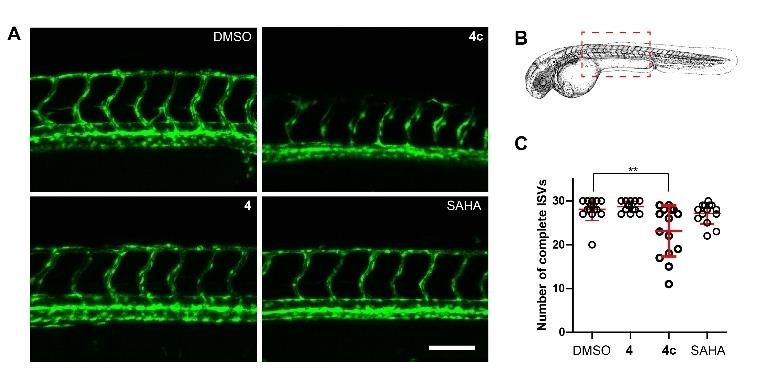
实体瘤患者中的预后与肿瘤血管有关,而HDAC与肿瘤血管生成密切相关。动物实验和临床结果都证实了,SAHA具有显著的抗血管生成活性。2μM的化合物4、4c和SAHA都显示了在斑马鱼中体内的抗血管活性,其中铑化合物4c显著减少了新血管生成,如图4所示。并且蛋白质印迹法发现,化合物4和4c都下调了VEGFR2血管内皮生长因子受体-2,减少了VEGFA血管内皮生长因子A。
图4.斑马鱼中干血管成像 图片来源:Angew. Chem. Int. Ed
总结
作者将不同活性的官能团组合在一个分子中,设计了靶向HDACs的多重药理学化合物。借鉴了SAHA的结构,设计合成了具有-吡啶硫代酰胺和异羟肟酸结构的化合物4及金属络合物,可以抑制HDAC。进一步药理实验发现,有机铑金属络合物4c具有较低的溶血活性,可以抑制斑马鱼血管的新生,下调了血管内皮生长因子受体-2。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!















No comments yet.