本文来自Chem-Station日文版,翻译投稿 张寻
本期热点研究,我们邀请到了东京农工大学工学学院的谷藤凉博士。
谷藤同学所在的大栗研究室采用全新的策略,通过多环多官能团天然物质的全合成,来进行生物化学方面的研究。此次研究不仅使用了人工合成手段,同时也使用了天然合成手段,即借助酶的力量。通过这样的方法,就可以较为有效地合成难以合成的沙弗拉霉素类物质。本次研究成果于前段时间发表在了J. Am. Chem. Soc.以及新闻刊物中。
Chemo-enzymatic Total Syntheses of Jorunnamycin A, Saframycin A, and N-Fmoc Saframycin Y3
Tanifuji, R.; Koketsu, K.; Takakura, M.; Asano, R.; Minami, A.; Oikawa, H.; Oguri, H.J. Am. Chem. Soc. 2018, 140, 10705. DOI: 10.1021/jacs.8b07161
我们从研究室的负责人大栗博毅教授那里听到了他对于谷藤同学的评价。究竟谷藤同学是如何顽强地挑战难关,且最终完美地取得了成果呢?请大家继续阅读。
“谷藤他可以吗?当时的我仅凭着直觉,就托付给了他一个难度很高的课题。酶反应的不确定性要素特别多,放大实验的操作也非常困难。酶这种东西特别娇嫩,很难对付,且研究者在实验过程中十分容易被不安定的中间体玩弄于股掌之间,对于常人来说根本没法坚持下去。这个实验也因此持续了好多年都没有结果。谷藤首先确立了合理的假说,一边不断地进行实验,一边积累经验和教训。他克服了一个个难关,且在此过程中磨练出了敏锐的观察力和实验能力,取得了很大的进步。
因为农工大的人事变动,研究室计划一系列生物化学实验都不得不借用其他研究室的设备。在其他研究室的老师和学生们的帮助下,经过不断探索,我们终于有了突破,成功打开了化学-酶合成的大门。同时在谷藤事无巨细的性格以及活跃表现的推动下,研究室成员养成了热爱实验,互相学习的习惯。因为最近得到了参加大津会议(注:日本有机化学界著名学术研讨会议)的机会,意气风发的谷藤君大胆地采用自己的想法,进行了调控生物碱与生物高分子之间相互作用方面的研究。他是我寄予很大期望的青年研究者之一,希望他可以在研究舞台上更加活跃,更有担当。”
Q1. 在本次访谈中您想和大家分享怎样的研究呢?请简单说明一下
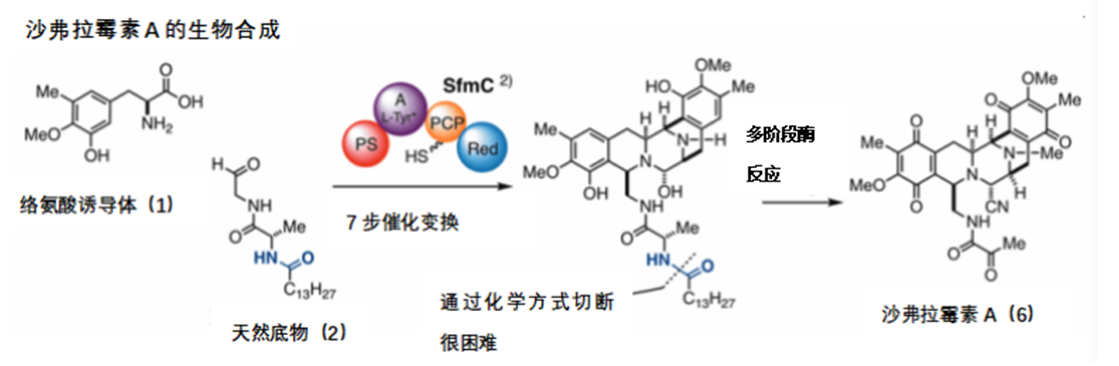
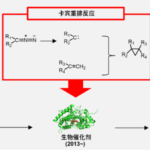
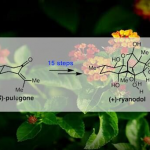
我们通过融合一次性构建多环结构的酶合成以及可以自由改变底物和中间体的有机合成,从而以化学-酶的混合方式合成沙弗拉霉素类物质。一般情况下,酶SfmC以络氨酸诱导体1(注:化学物质后的数字为图中所对应数字)和豆蔻酸合成的二肽醛2为天然底物,形成和沙弗拉霉素类物质相同的五环结构。
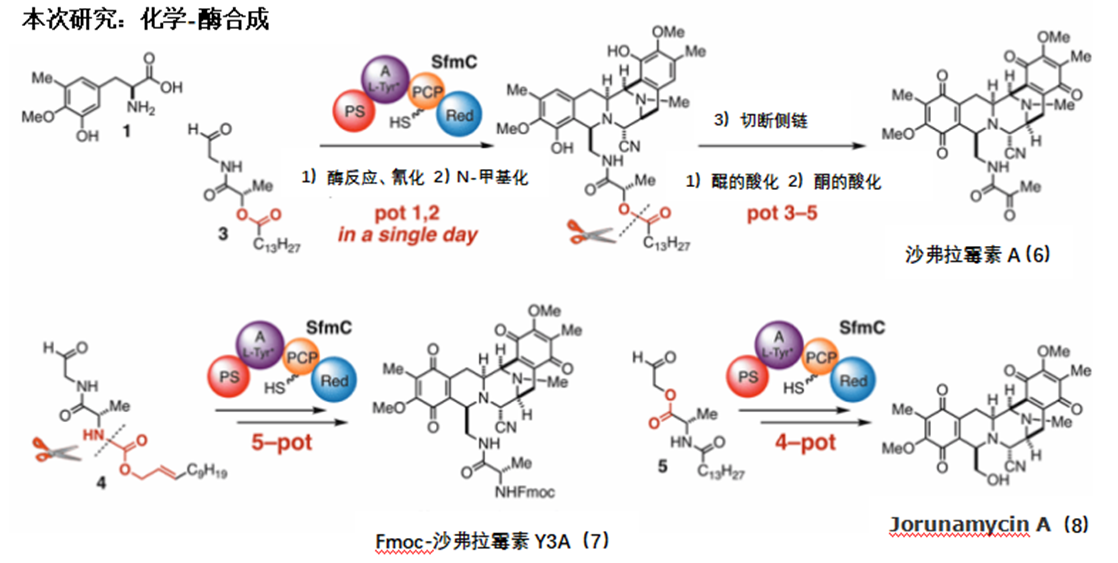
本次研究中,我们通过改造含有醛基的底物2,设计并合成了3~5所示的三种非天然物质。同时,在构建好物质结构以后,通过化学合成的方式将酶反应不可或缺的长链脂肪酸的侧链切断,并进行官能团的变换。使用3~5这三种非天然物质,我们成功地用五步反应合成了具有抗癌活性的沙弗拉霉素A6以及沙弗拉霉素Y3 Fmoc保护体7,用四步反应合成了Jorunamycin A(8)。
本次研究所使用的酶SfmC,可以连续催化7段反应,可以说是相当特别。其官能团众多,具有复杂的五环结构。有关合成SfmC酶的反应以及合成底物1的反应,请参考本研究室的论文。
Q2.有关本次研究主体,有没有什么让您感觉特别辛苦和烧脑呢?
SfmC的失活速度特别快,并且变换那几种非天然底物也是个棘手的工作,以至于刚开始试验的时候,酶反应的收率连5%都不到。为了改善收率,我们把原本需要花8个小时的SfmC提炼缩短到了两个小时。为尽可能地防止酶失去活性,我们在提炼完后马上就开始酶反应。并且我们认为,因通过酶反应生成的五环结构是仲胺,所以会导致收率比较低。于是我们在不分离仲胺中间体的前提下进行氮甲基化反应并且进行提炼。做这些事情真的是费了无数的工夫。但功夫不负有心人,我们得到了良好的五环性目标产物,收率也提升了一个台阶。在硕士一年级的冬天提炼HPLC时,目标化合物出现了特别尖的峰。那个瞬间至今还清晰的印在我的脑海中。
Q3.在研究的时候遇到过怎样的困难呢?又是怎样克服的呢?
我们发现,在使用经复杂的生物合成而得到的酶来进行变换时,合成天然化合物已经不是难事。虽然最终得到的合成路径看似很简单,但为了得到这个结果,我们忍受着繁重的工作,还要重复进行试验,不断修正错误。因为分子量超过16万的巨大生物合成酶SfmC失活非常快,所以在每次酶反应之前都要进行配制。为了最大程度防止酶失活,我只能每天把自己关在4摄氏度的冷库里来提炼酶。多亏了在北海道培养出来的耐寒体质。
说实话,使用从大肠杆菌中亲手提炼的酶,将自己合成的底物变成复杂的化合物的过程,真的开心到无以言表。我在实验中不断地试错,慢慢地离合成天然有机物的目标越来越近,磨练了自己不轻易言弃的精神,从而能够克服堆积如山的课题压力。
Q4.将来想研究化学的哪个方向呢?
我想自由地在多个方向进行研究,并且开拓新的研究方向。在微生物二次代谢产物的生物合成的相关研究中,其所表现出的进化之奇妙让我十分感兴趣。并且,本次研究课题的后续研究中,天然物质的魅力也令人叹服。最近一段时间我们验证了沙弗拉霉素类物质和生物分子之间的相互作用,每天都沉浸在微生物在内的生物世界中。我感到探寻本质是有机化学的根本任务。有机化学的博大精深让我为之着迷。虽然学识尚有不足,但我仍然希望可以从自己的兴趣出发,不断在化学的海洋中遨游。
Q5.最后,有什么想对各位读者说的吗
最初合成天然物质是在硕士二年级的6月份。实则从硕士二年级的10月开始一直到博士一年级的6月,大约八个月的时间,天天过的都是酶反应的收率在十分之一左右的日子。酶没有什么问题,且底物合成和缓冲液的配制什么的也很正常,可即使如此,实验的情况就是不乐观。但我倒也没因此有什么挫败感。因为我感觉这是在研究的时候必然会发生的事。或许现在会有很多人整日面对着毫无进展的研究愁眉不展。但仔细想想,难道这不是个锻炼机会吗,通过锻炼,你可以成为更优秀的研究员,成为更优秀的人。对于我来说,每当研究进入瓶颈期的时候,我就会想起那些艰难的日子,然后重拾自信,继续冷静地思考下一步的策略。同时也要注意适当休息。让我们一起为振兴化学而奋斗吧。
最后,感谢给我这次访谈机会的化学空间的所有工作人员。除此之外,本次的研究课题也是在多方支持下才能有今天的成果。不仅是我的导师,北海道大学工学部的大利徹教授、小笠原泰志助教、理学部的尾濑丰之副教授、农学部的福士江里博士也为我提供了很大的帮助。并且,现任北卡罗来纳大学教堂山分校教授的早出广司老师以及东京农工大学的池袋·津川·浅野研究室的老师和同学们,在研究室搬迁以后,在生物化学实验方面为我提供了诸多帮助。感谢大家一直以来毫不吝惜地让我借用实验室!
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!






















No comments yet.