- 概要
狄尔斯–阿尔德反应是[4+2]环加成反应中最具代表的,由共轭双烯与亲双烯体构建环己烯骨架的经典反应。反应有良好的立体、位置选择性。
该反应常作为合成环状化合物(特别是六元环)的首选战略,在诸多反应中它的实用性很显著。
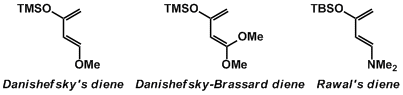
Danishefsky’s diene(北原-Danishefsky’s diene) 双烯与一般的双烯相比,有更好的反应性及位置选择性。因此,是熟为人知的有机合成试剂,类似的双烯还有Danishefsky-Brassard diene、 Rawal diene等。
 Otto Diels 和Kurt Alder两位化学家,由于对发现这一反应的贡献,于1950年获得诺贝尔化学奖。
Otto Diels 和Kurt Alder两位化学家,由于对发现这一反应的贡献,于1950年获得诺贝尔化学奖。
- 基本文献
・Diels, O.; Alder, K. Liebigs Ann. Chem. 1928, 460 , 98 DOI:10.1002/jlac.19284600106
・Kloetzel, M. C. Org. React. 1948, 4, 1.
・Holms, H. L. Org. React. 1948, 4, 60.
・Martin, J. G. Chem. Rev. 1961, 61, 537. DOI:10.1021/cr00013a013
・Sustman, R. et al. Angew. Chem. Int. Ed. Engl. 1980, 19, 779.
・Oppolzer, W. Comprehensive Organic Synthesis 1991, 5, 315.
・Roush, W. R. Comprehensive Organic Synthesis 1991, 5, 513.
・Yamabe, S.; Minato, T. J. Org. Chem. 2000, 65, 1830. DOI: 10.1021/jo9919310
・Nicolaou, K. C.; Synder, S. A.; Montagnon, T.; Vassilikogiannakis, G. Angew. Chem. Int. Ed. 2002,41, 1668. [Abstract]
- 反应机理
通常,带有给电子基的双烯体和带有吸电子基的亲双烯体进行反应。因为前沿轨道(双烯的HOMO和亲双烯体的LUMO)的能量差越小,能够使轨道相互作用而稳定,从而使反应更容易进行(通常电子要求型)。同理,亲双烯体带有给电子基,共轭双烯带吸电子基的反应也容易进行(反电子要求型)。
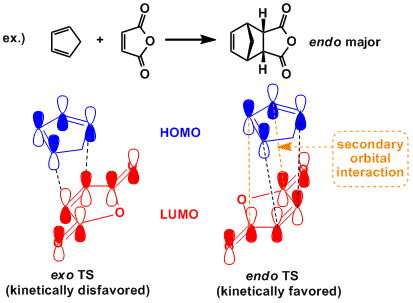
反应是按协同反应顺式加成来进行的,优先生成endo加成产物(endo规则)。通常电子要求型的情况下二次轨道相互作用大致能解释这一规则,但endo/exo选择性也受立体影响,根据不同底物,完全选择生成exo产物的例子也有报道。除此之外分子内的Diels-Alder反应由于环状结构固定,构型自由度较低,也不完全适用endo规则。
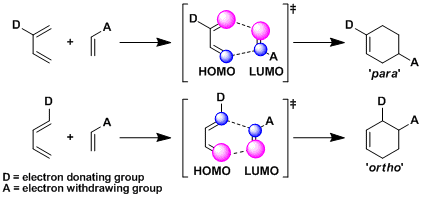
根据有机电子理论的推测,Diels-Alder反应的加成产物更容易使置换基处于邻位或对位(邻、对位规则)。具体可由前沿轨道理论来说明,即HOMO-LUMO的系数大的反应点易于相互重叠而加成。
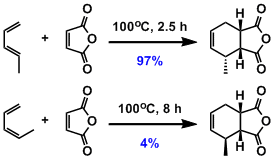
环状过渡态的双烯是s-cis(cisoid)结构时可加成,s-trans(transoid)结构则不能发生Diels-Alder反应。如下反应中,Z-1,3-pentadiene很难转变为s-cis结构,反应性与E式相比明显低下。
- 反应实例
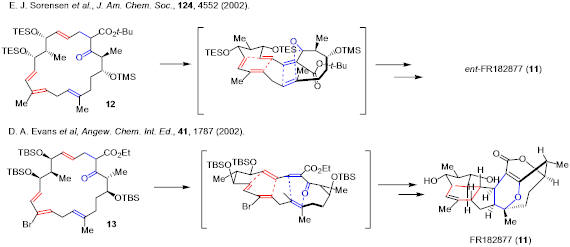
近年来,利用Diels-Alder反应进行仿生全合成的研究多有报道,如Sorensen及Evans两个研究组实现了分子内Diels-Alder反应合成FR82877的全合成。
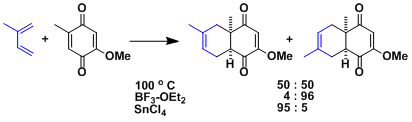
已经知道由于lewis酸而导致的位置选择性不同的例子(螯合作用、或与底物的结合位置变化造成)。
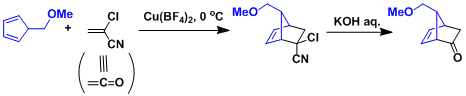
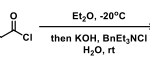
前列腺素类的合成:a-氯丙烯腈在Diels-Alder反应中等同烯酮的反应。
- 实验步骤
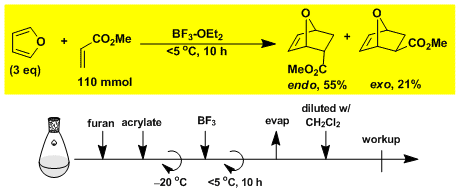
用呋喃与丙烯酸甲酯的Diels-Alder反应[1]
- 实验技巧
- 参考文献


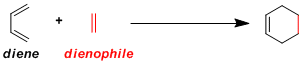
















No comments yet.