本次介绍的论文中报道了使用镍催化剂的链烯基酰胺的1,2-二芳基化反应的开发。通过使用富马酸酯作为配体,可以很简单的将含有酰胺基团的烯烃进行二芳基化。
非共轭烯烃的1,2-二芳基化反应
烯烃是一种非常有用的结构单元,可通过引入取代基构建复杂的分子结构。近年来,区域选择性地将两种类型的官能团引入烯烃中的方法学的开发受到研究人员的关注。其中,使用钯或镍催化剂催化的烯烃的1,2-二芳基化反应已经被报道[1]。要实现该反应,最大的关键是抑制底物-金属活性种的β–氢消除。有许多能够产生π-烯丙基和π-苄基配合物的1,3-二烯或苯乙烯的1,2-二芳基化由于能够稳定活性中间体,因此被研究报道的比较多(图1A)[2]。另外,还有一些报道表明取向基团的烯烃如喹啉酰胺,亚胺和吡啶基硅烷,可通过与烷基金属物种配位从而实现稳定中间体的作用,抑制β–氢消除生成1,2-二芳基化合物(图1B)[3]。
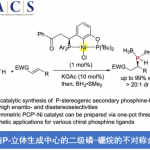
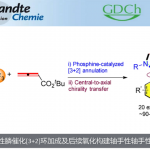
这次、Engle助理教授等人,通过使用具有富马酸酯作为配体的镍催化剂,成功地对具有更一般的酰胺基团的烯烃进行1,2-二芳基官能团化(图1C)。
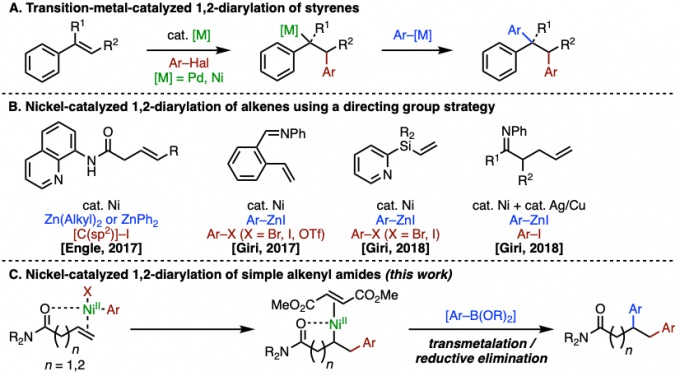
图1.烯烃的1,2-二芳基化反应
“Nickel-Catalyzed 1,2-Diarylation of Simple Alkenyl Amides”
Derosa, J.; Kleinmans, R.; Tran, V. T.; Karunananda, M. K.; Wisniewski, S. R.; Eastgate, M. D.; Engle. K. M. J. Am. Chem. Soc.2018,140, 17878.
DOI: 10.1021/jacs.8b11942
论文作者介绍

履历:
2003–2007 B.S. in Chemistry, Economics, Mathematics, and Statistics University of Michigan (Prof. Adam J. Matzger)
2008–2013 Ph.D. in Chemistry, The Scripps Research Institute (Prof. Jin-Quan Yu)
2008–2013 D.Phil. in Biochemistry,University of Oxford (Prof. Veronique Gouverneur and John M. Brown)
2013–2015 NIH Postdoctoral Fellow,Caltech (Prof. Robert H. Grubbs)
2015–Assistant Professor of Chemistry, The Scripps Research Institute
研究内容:烯烃的区域选择性官能团化方法学开发
论文概要
该反应通过在异丁醇溶剂中、富马酸二甲酯作为配体的镍催化剂的存在下、加入氢氧化钠,在室温下使链烯基酰胺1,碘苯2和芳基硼酸酯3混合进行反应,从而产生高产率的1,2-二芳基化产物(图2A)。本反应的底物适用范围广、无论芳基硼酸酯具有给电子取代基或吸电子取代基,反应都可以以良好的收率进行。该反应适用于具有给电子取代基的碘代芳烃,可以中~高产率获得所需产物。另外β,γ–与γ,δ–链烯烃酰胺同样适用该反应。值得注意的是,即使在酰胺氮上具有各种烷基取代基,反应也能顺利进行。
DFT计算表明,羰基作为导向基团,富马酸二甲酯(一种缺电子的烯烃配体)促进了催化剂循环的还原消除过程。因此,作者推定的反应机理如下所示(图2B)。首先,将碘代芳烃氧化加成到镍(0)催化剂中,然后与链烯基酰胺配位(I)。接下来,通过配位插入和配体交换,形成镍循环(II)。接下来与芳基硼酸酯进行金属转移反应后(III)、再进行还原消除得到1,2-二芳基化产物(IV)。
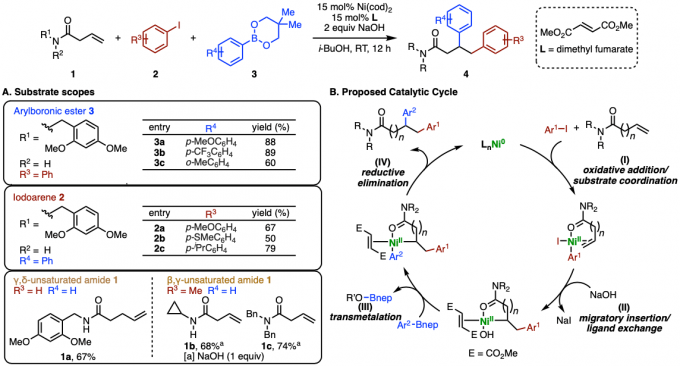
图2. (A) 底物适用范围 (B) 推定反应机理
综上所述、使用镍催化剂和富马酸二乙酯、实现了非共轭链烯基酰胺的1,2-二芳基化反应。预期通过酰胺键的转换可以通过本手法进行复杂化合物的合成。
参考文献
- (a) Derosa, J.; Tran, V. T.; van der Puyl, V. A.; Engle, K. M. AldrichimicaActa 2018, 51, 21.(b)Giri, R.; KC, S. J. Org. Chem.2018, 83, 3013.DOI: 10.1021/acs.joc.7b03128
- (a) Stokes, B. J.; Liao, L.; de Andrade, A. M.; Wang, Q.; Sigman, M. S. Org. Lett. 2014, 16, 4666. DOI: 10.1021/ol502279u (b)Urkalan, K. B.; Sigman, M. S. Angew. Chem., Int. Ed. 2009,48, 3146.DOI: 10.1002/anie.200900218
- (a) Derosa, J.; Tran, V. T.; Boulous, M. N.; Chen, J. S.; Engle, K. M. J. Am. Chem. Soc.2017, 139, 10657. DOI: 10.1021/jacs.7b06567 (b) Shrestha, B.; Basnet, P.; Dhungana, R. K.; KC, S.; Thapa, S.; Sears, J. M.; Giri, R. J. Am. Chem. Soc.2017, 139, 10653.DOI: 10.1021/jacs.7b06340 (c)Thapa, S.; Dhungana, R. K.; Magar, R. T.; Shrestha, B.; KC, S.; Giri, R. Chem. Sci.2018, 9, 904.DOI: 10.1039/c7sc04351a (d)Basnet, P.; KC, S.; Dhungana, R. K.; Shrestha, B.; Boyle, T. J.; Giri, R. J. Am. Chem. Soc. 2018, 140, 15586. DOI: 10.1021/jacs.8b09401
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.