译自Chem-Station网站日本版 原文链接:内部アルコキシ効果 Inside Alkoxy Effect
翻译:炸鸡 校对:Jiao Jiao
简介
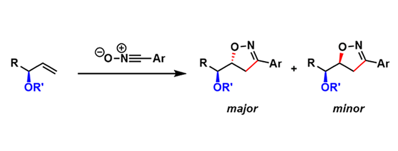
手性链状烯丙基醚的碳碳双键发生1,3-偶极环加成反应时,反应被发现具有立体选择性。对于这一立体选择性的出现,一个比较有说服力的解释是Inside Alkoxy Effect。
基本文献
- Stork, G.; Kahn, M. Tetrahedron Lett. 1983,24, 3951. doi:1016/S0040-4039(00)88233-7
- Houk, K. N.; Moses, S. R.; Wu, Y. D.; Rondan, N. G.; Jager, V.; Schohe, R.; Fronczek, F. R. Am. Chem. Soc.1984, 106, 3880. doi:10.1021/ja00325a040
- Houk, K. N.; Rondan, N. G.; Wu, Y.-D.; Metz, J. T.; Paddon-Row, M. N. Tetrahedron1984, 40, 2257. doi:1016/0040-4020(84)80009-5
- Cha, J. K.; Christ, W. J.; Kishi, Y. Tetrahedron1984, 40, 2247. doi:1016/0040-4020(84)80008-3
- Vedejs, E.; McClure, C. K. Am. Chem. Soc. 1986, 108, 1094. doi:10.1021/ja00265a048
- Houk, K. N.; Dhu, H. Y.; Dong, Y.; Moses, S. R. Am. Chem. Soc.1986, 108, 2754. doi:10.1021/ja00270a044
- Raimondi, L.; Wu, Y.-D.; Brown, F. K.; Houk, K. N. Tetrahedron Lett.1992, 33, 4409. doi:1016/S0040-4039(00)60096-5
- Haller, J.; Strassner, T.; Houk, K. N. Am. Chem. Soc.1997, 119, 8031. doi:10.1021/ja971342g
- Annunziata, R.; Benaglia, M.; Cinquini,M.; Cozzi, F.; Raimondi, L. J. Org. Chem.1998, 1823. [abstract]
- Raimondi, L.; Benaglia, M. J. Org. Chem.2001, 1033. [abstract]
- Patel, A.; Vella, J. R.; Ma, Z.-X.; Hsung, R. P.; Houk, K. N. Org. Chem.2015, 80, 11888. doi:10.1021/acs.joc.5b02085
<review>
- 斎藤 清機, 有機合成化学協会誌, 1992, 50, 316. doi:5059/yukigoseikyokaishi.50.316
- Eksterowicz, J. E.; Houk, K. N. Rev.1993, 93, 2439. doi:10.1021/cr00023a006
- Mengel, A.; Reiser, O. Rev.1999, 99, 1191. doi:10.1021/cr980379w
发现历程
1983年,Gilbert Stork等人首次提出了出现于四氧化锇氧化体系内的Inside Alkoxy Effect。随后在1984年Kendall Houk等人将Inside Alkoxy Effect作为氧化腈发生1,3-偶极环加成反应的计算化学佐证。
Kendall N. Houk (1943-)
反应机理
仅仅用1,3-烯丙基的位阻的原因来解释是不够的,还需要用立体电子效应来解释。
碳碳单键是可以自由旋转的,一旦烷氧基α碳的C-O σ*反键轨道与C=C的π轨道共轭,C=C键上的电子密度就会下降,比较难与亲电试剂发生反应了。反之,若取代基R的C-C的σ轨道越能与C=C π轨道共轭,反应越容易进行。
既要C-C的σ轨道与C=C π轨道最大程度共轭又要空间位阻尽可能地小,满足着这两个条件的立体构象是这样的:取代基R与双键所在的平面垂直,烷基R’面向双键朝里。当烯丙基醚呈现出这样的构象时,亲核试剂会从R基的反面进攻以减小位阻效应,如下图所示的中间态就能很好地解释最后的加成产物的立体构型。
反应案例
全合成的应用
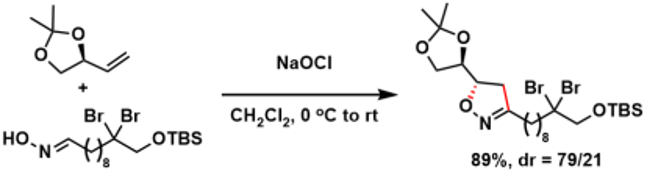
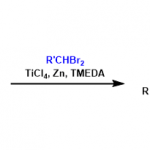
Bromodanicalipin A的合成[1]
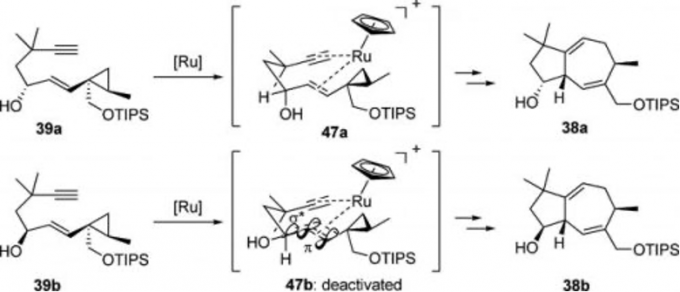
(+)-Frondosin A的合成[2]:Ru催化的[5+2]环加成中,用1,3-烯丙基的Inside Alkoxy Effect能很好地说明最终产物的立体选择性(第一行的中间态占优势)。
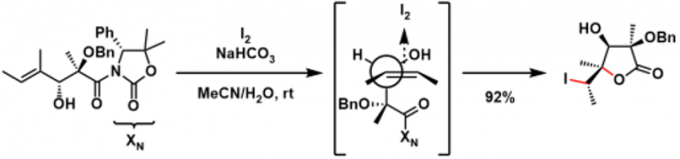
(+)-Citreoviral的全合成[3]:碘内酯化反应(Iodolactonization)产物的立体构型也能用Inside Alkoxy Effect解释。
参考文献
- Fischer, S.; Huwyler, N.; Wolfrum, S.; Carreira, E. M. Chem. Int. Ed.2016, 55, 2555. doi:10.1002/anie.201510608
- Trost, B. M.; Hu, Y.; Horne, D. B. Am. Chem. Soc.2007, 129, 11781. doi:10.1021/ja073272b
- Murata, Y.; Kamino, T.; Aoki, T.; Hosookawa, S.; Kobayashi, S. Chem. Int. Ed.2004, 43, 3175. doi:10.1002/anie.200454212
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载




















No comments yet.