作者:石油醚
引言
近日,Ludwig-Maximilian University的Burkhard Krumm教授等人Burkhard Krumm教授等人开发了一种立方烷-1,2,4-三羧酸三甲酯的改进型克级合成法,支撑该三取代体系的系统性研究与衍生化,成功制备并全面表征了多种三取代立方烷衍生物,包括首例含能三取代立方烷(4、5、6)。
Convenient Access to Trisubstituted Cubanes and Nitrated Derivatives
Andreas BartonekThomas M. Klapötke*Burkhard Krumm*
Org. Process Res. Dev. 2026. DOI : 10.1021/acs.oprd.5c00479
正文
立方烷母体分子具有高达622 kJ/mol的环张力(约78 kJ/mol/碳),低于prismane(95 kJ/mol/碳)。此外,立方烷具有较好的热力学稳定性,且分解温度可达220°C。然而,prismane则极易剧烈分解。
除了立方烷本体外,理论和计算表明,高取代立方烷的密度会更高。尽管1,4-二取代立方烷已被广泛研究,但三取代及以上衍生物仍鲜有实验报道。目前,现有的研究集中于硝基立方烷和四取代立方烷。特别的是,高取代结构的价值在于可进一步功能化并提升能量性能。四取代立方烷需多步合成,涉及保护基与金属有机反应。含能基团的三取代立方烷尚无实验报道,仅有三硝基立方烷等计算研究。此前发展的氯自由基引发—氯羰基化路线为高取代立方烷提供了可行路径,Eaton曾沿用该策略,并在近期工作进一步优化使用9 W UV-B,显著提升操作安全性。
近日,Ludwig-Maximilian University的Burkhard Krumm教授等人开发了一种适用于三取代立方烷前体的简化合成,并首次制备、表征多种新型三取代立方烷衍生物。
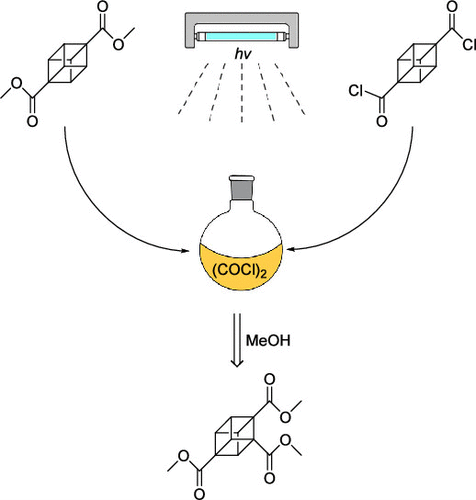
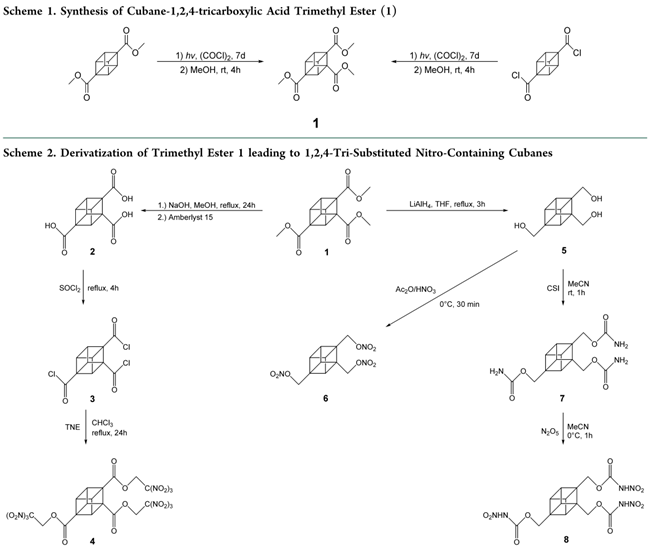
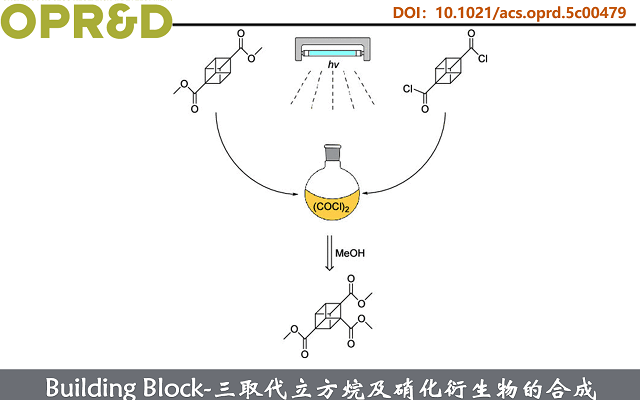
首先,作者对其前体进行合成(Scheme 1)。即1)在立方烷-1,4-二甲酸二甲酯和草酰氯的体系下用9 W UV-B灯室温照射7天,即可高效制备关键前体,立方烷-1,2,4-三甲酸三甲酯(1,20 g 规模,80%产率)。其效果与150 W Hg灯照射的相当。值得注意的是,反应时持续释放HCl和CO,通过标准甲醇淬灭/柱层析即可纯化1。对应二酰氯反应更快:5天达~80%,7天(10 g规模)产率升至93%,进而证实其活性高于二甲酯。 进一步延长辐照(>7天)可少量生成立方烷-1,2,4,7-四甲酸四甲酯(NMR鉴定并分离),表明该路径适用于四取代衍生物合成。
其次,对前体1进行相关衍生化(Scheme 2)。即1)1经碱性水解及离子交换树脂酸化,以94%产率得水溶性立方烷-1,2,4-三羧酸(2);继而用SOCl₂氯化,首次获得可分离的立方烷-1,2,4-三羰基氯(3)(此前仅NMR检出)。3与过量的三硝基乙醇(TNE)回流2天,经柱层析+重结晶以30%的产率获得立方烷-1,2,4-三羧酸三(2,2,2-三硝基乙酯)(4);2)1经LiAlH₄还原,以96%产率得立方烷-1,2,4-三甲醇(5);5再经HNO₃/Ac₂O硝化,得立方烷-1,2,4-三甲基硝酸酯(6);3)化合物5与氯磺酰异氰酸酯(CSI)反应,以96%产率高效制得立方烷-1,2,4-三甲基氨基甲酸酯(7)。7的硝化可生成目标硝基氨基甲酸酯(8)(NMR检测获得,并未分离纯化)。
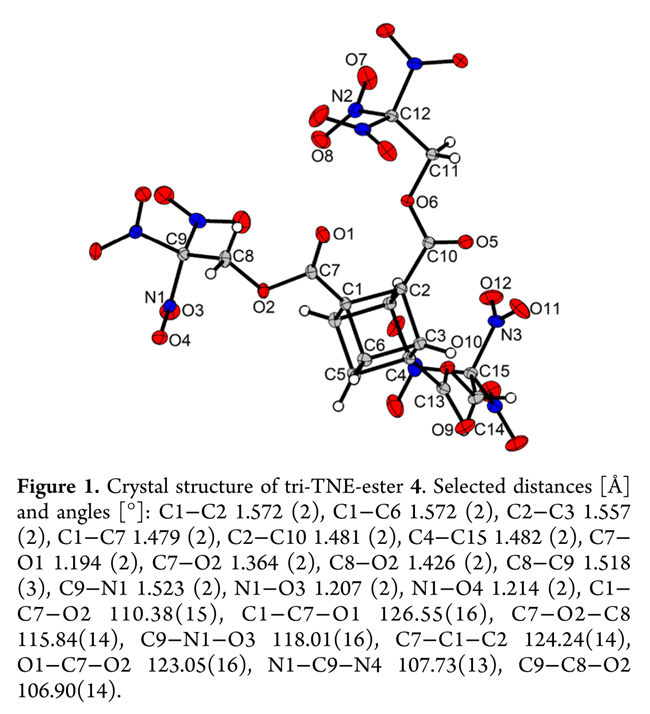
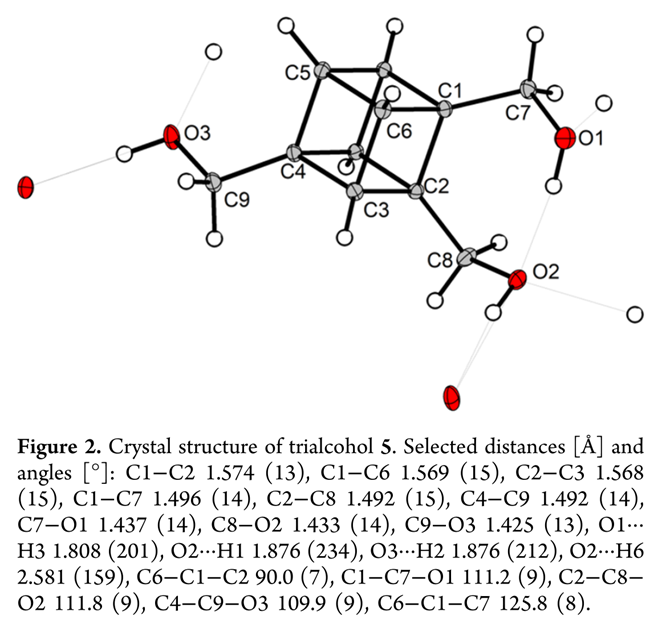
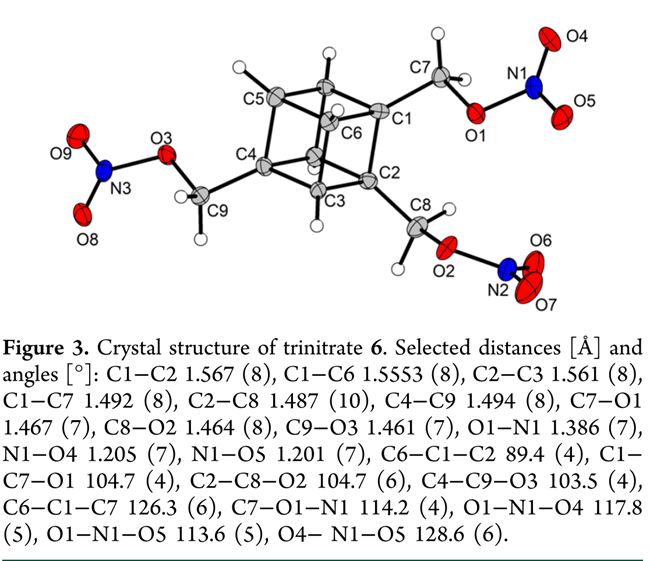
接下来,对上述部分化合物进行相关测试。即1,2,4-取代立方烷的对称性使其在所有¹H 和 ¹³C{¹H} NMR谱中呈现特征性共振模式:¹H谱中CH信号位于3.88–4.85 ppm,为积分比2:2:1的三个多重峰,其中一组略位移;该规律同样适用于1、4、5、6、7中CH₂/CH₃基团。¹³C{¹H}谱清晰显示每个碳对应三组共振。¹⁵N谱(化合物4和6)亦呈三重峰模式,每组取代基给出三个三重峰,其中两组化学位移高度接近;2)单晶X射线衍射分析表明: 4的晶体结构(无色棒状晶体,P2₁/c,ρ = 1.85 g·cm⁻³,173 K,Figure 1)与二取代TNE酯高度相似,键长/键角基本一致;微小偏差(如C7−C1−C2角减小≈1°)源于三取代基的空间拥挤;5的晶体(无色块状晶体,P2₁/c,ρ = 1.38 g·cm⁻³,109 K,Figure 2)中三个羟基形成强分子内O···H氢键(O1···H3、O2···H1、O3···H2,d = 1.808–1.876 Å),另有一弱接触(O2···H6,d = 2.581 Å);立方烷骨架完好(C−C ≈ 1.57 Å,∠C−C−C ≈ 90°);6(无色片状晶体,P2₁,ρ = 1.64 g·cm⁻³,173 K,Figure 3)中C−O键(1.492 Å)较5中(1.437 Å)延长,归因于硝基吸电子效应;其硝酸酯基N−O键呈典型不对称分布(O₁−N₁ = 1.39 Å,N₁−O₄ = 1.21 Å),反映O₁−N₁单键与N₁=O₄双键特征。
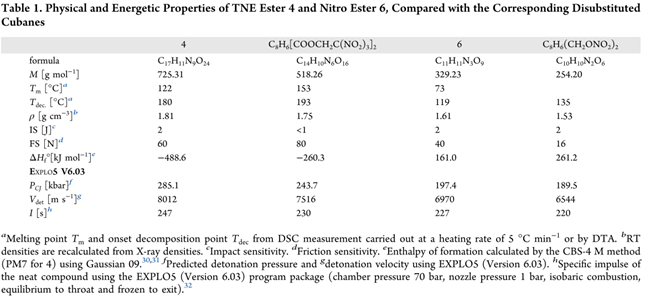
最后,对三取代TNE酯(4)与硝基酯(6)的物理及能量性质测定结果(Table 1),并与对应二取代立方烷酯对比。其中,4的密度达1.81 g·cm⁻³,较二取代TNE酯高0.06 g·cm⁻³;撞击感度略降,摩擦感度升高。 6密度较二取代二硝酸酯提高0.08 g·cm⁻³,其首次观测到明确熔点(二取代硝基酯通常无熔点),熔融先于分解,故摩擦感度降低。 4与6的含能参数均提升,但热稳定性下降,其源于更强吸能取代基及增大的环张力。
结论
Burkhard Krumm教授等人开发了一种立方烷-1,2,4-三羧酸三甲酯的改进型克级合成法,支撑该三取代体系的系统性研究与衍生化,成功制备并全面表征了多种三取代立方烷衍生物,包括首例含能三取代立方烷(4、5、6)。其中,4、5和6的单晶结构已获解析。相较于二取代类似物,三取代含能立方烷热稳定性降低,但密度与能量性能更高,源于更高的堆积密度及更多含能基团引入所致的环张力增大。目前,更高取代度立方烷体系的研究正在推进,有望获得性能更优的新材料。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841
请登陆TCI试剂官网查看更多内容
https://www.tcichemicals.com/CN/zh/

















No comments yet.