作者:石油醚
引言
流感(influenza或flu)仍是全球重大的公共卫生问题,其季节性暴发和周期性流行对医疗系统及社会运行造成显著负担。该疾病起病急骤,临床表现复杂多样,每年在全球范围内导致数以百万计的感染病例。长期以来,疫苗和神经氨酸酶抑制剂一直是防控流感感染的主要手段。尽管这些干预措施在控制流感传播方面发挥了重要作用,但仍面临持续挑战:一方面存在药物耐药性日益加剧的风险,另一方面亟需开发兼具高效性与快速起效特点的新型治疗药物。因此,开发新型抗病毒药物的目标在于提供高效且具有替代性的治疗方案,以应对当前面临的持续挑战。基于此,SHIONOGI & CO., LTD.和瑞士罗氏制药公司(Roche)合作共同研发了流感帽依赖型内切酶抑制剂玛巴洛沙韦(1)(baloxavir marboxil,Xofluza,BXM)。
玛巴洛沙韦(速福达,(Xofluza)):第一代合成路线
BXM设计思路来源于对HIV整合酶抑制剂多替拉韦的改造。除此之外,BXM(1)为前药,在体内经芳基乙酰胺脱乙酰酶代谢后转化为活性形式玛巴洛沙韦酸 (图1)。

图1 玛巴洛沙韦及活性成分
BXA结构包含两个主要核心单元:三环稠合的三嗪酮核与三环稠合的硫杂环庚烷核,二者均含有手性中心。经过化合物发现阶段,手性三嗪酮(16)以及BXA(2)均需要HPLC分离。HPLC分离适用于早期药物化学研究中目标化合物的快速分离,但其存在循环时间长、成本高等问题。因此,科学家开发了BXM工业合成的初代路线(图 2)
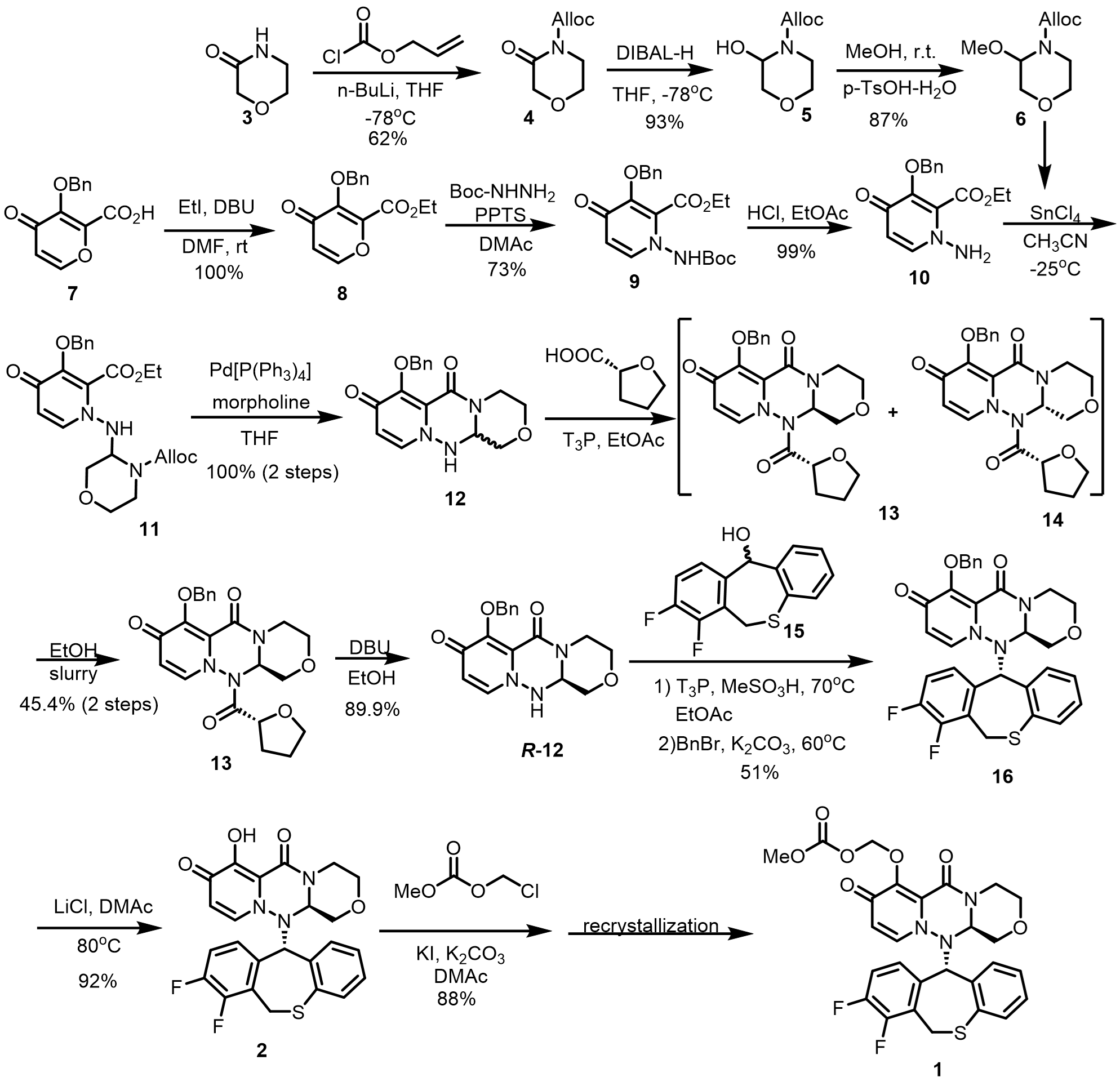
图2 BXM工业合成的初代路线
一代工艺路线中重点过程优化
1)12的手性拆分

图 3 12的手性拆分
首先,通过R–12与多种手性羧酸缩合(图3),考察是否可选择性析出所需非对映异构体固体。结果表明:1)R–12与羧酸17a和17b缩合产率较低;2)R–12与18a,18b,19a,19b的缩合产率较高,仅有产物 22 和 13 为固体化合物;3)以19a作为手性拆分剂,S–12与 19a 的缩合产物 25 为非晶态 14 的对映体,而 R–12与 19a 的缩合产物 14则为固体。进一步表明消旋体 12与 19a 缩合会生成可通过结晶分离的非对映体。
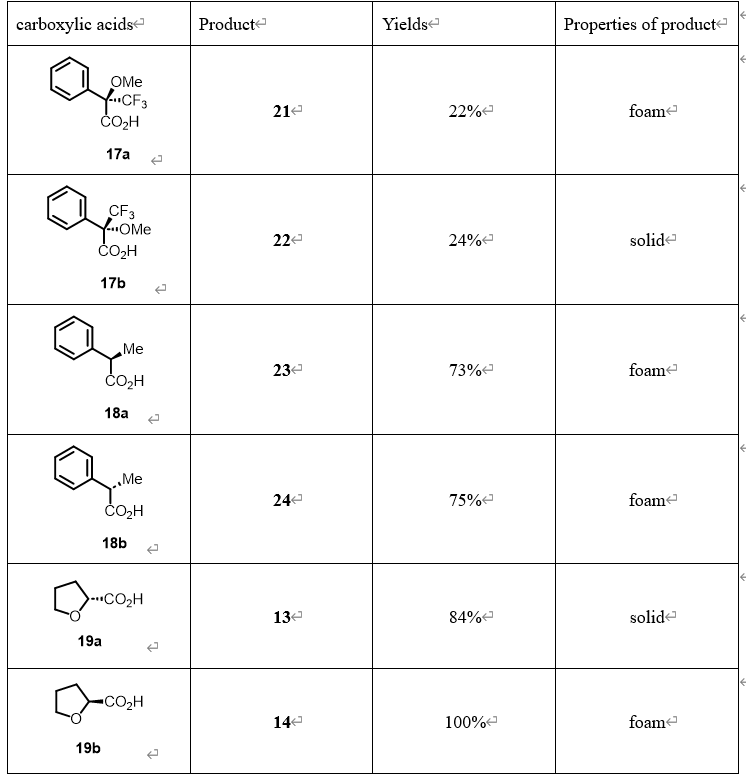
图 4 缩合反应及其性质
基于上述研究,开发了一条可用于放大合成R–12的工艺路线(图 5),即rac–12与 21a 缩合生成等量的非对映异构体 13 和 25,经过滤、DBU脱除手性拆分试剂和异丙醚重结晶,即可获得R–12。其中,25可通过过滤留在母液中,且其可通过DBU/BHT体系转化为rac–12,用于进一步拆分而降低成本。
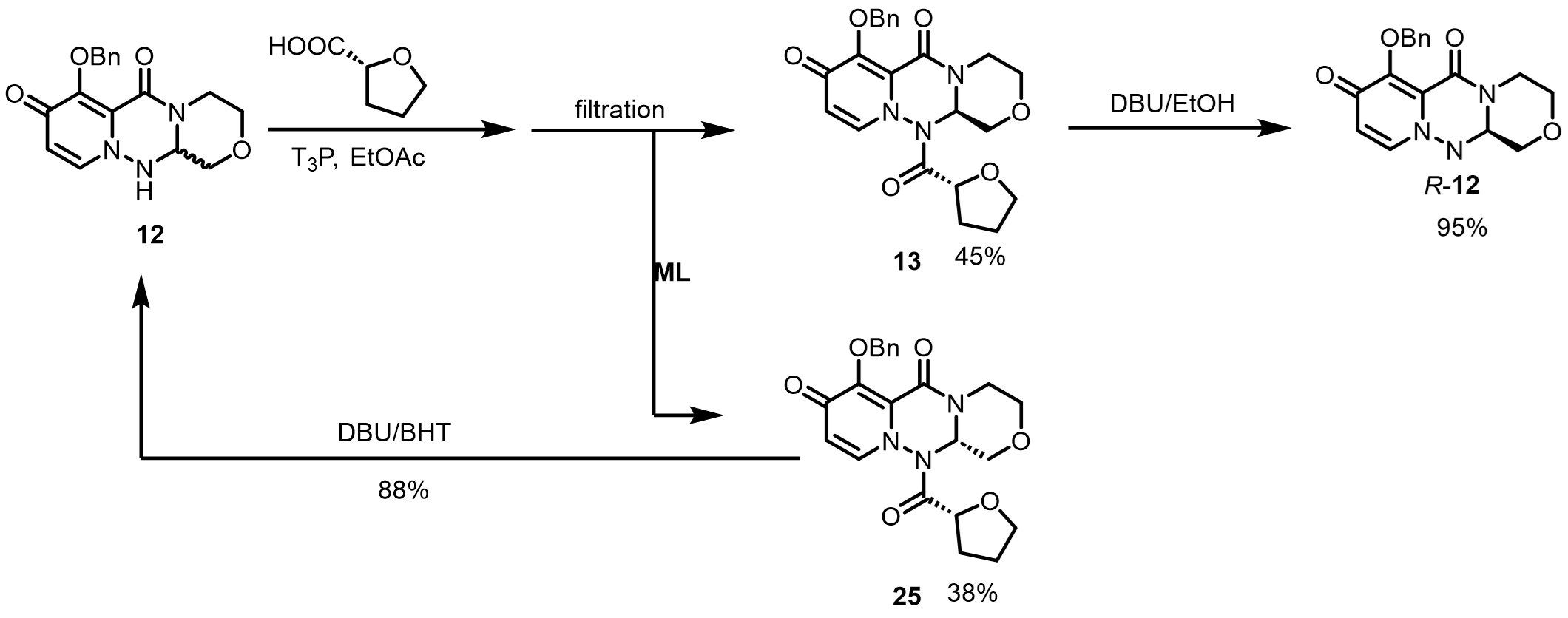
图 5 rac–12的光学拆分结果和25的再回收
2)中间体16的合成优化
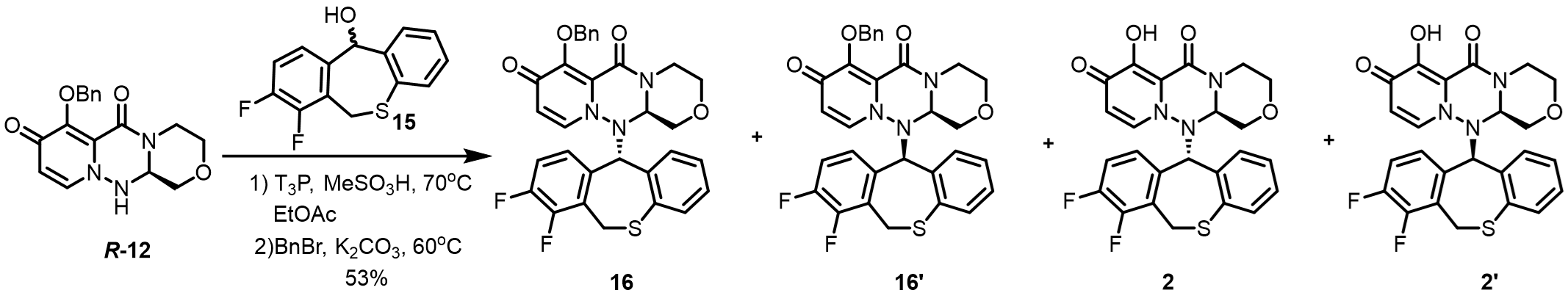
图 6 偶联反应优化
前期研究发现,R–12与15的主要的副产物是2和2′。经过进一步的优化发现了最佳的反应条件(图 6),即R–12 (1.0 eq.), 15 (1.2 eq.), T3P (1.5 eq.), EA (2. 5 BV), MsOH (1.8 eq.),在80℃下反应3h。偶联反应完成后,后处理得到含 16 和 2 的非对映异构体的粗油。为便于纯化,通过苄基化将 2 和 2′ 转化为 16和 16′。随后在 60% 乙酸乙酯/己烷中重结晶,以49%的产率获得16(16:16′ ≥ 99:1)。
CMC阶段放大合成
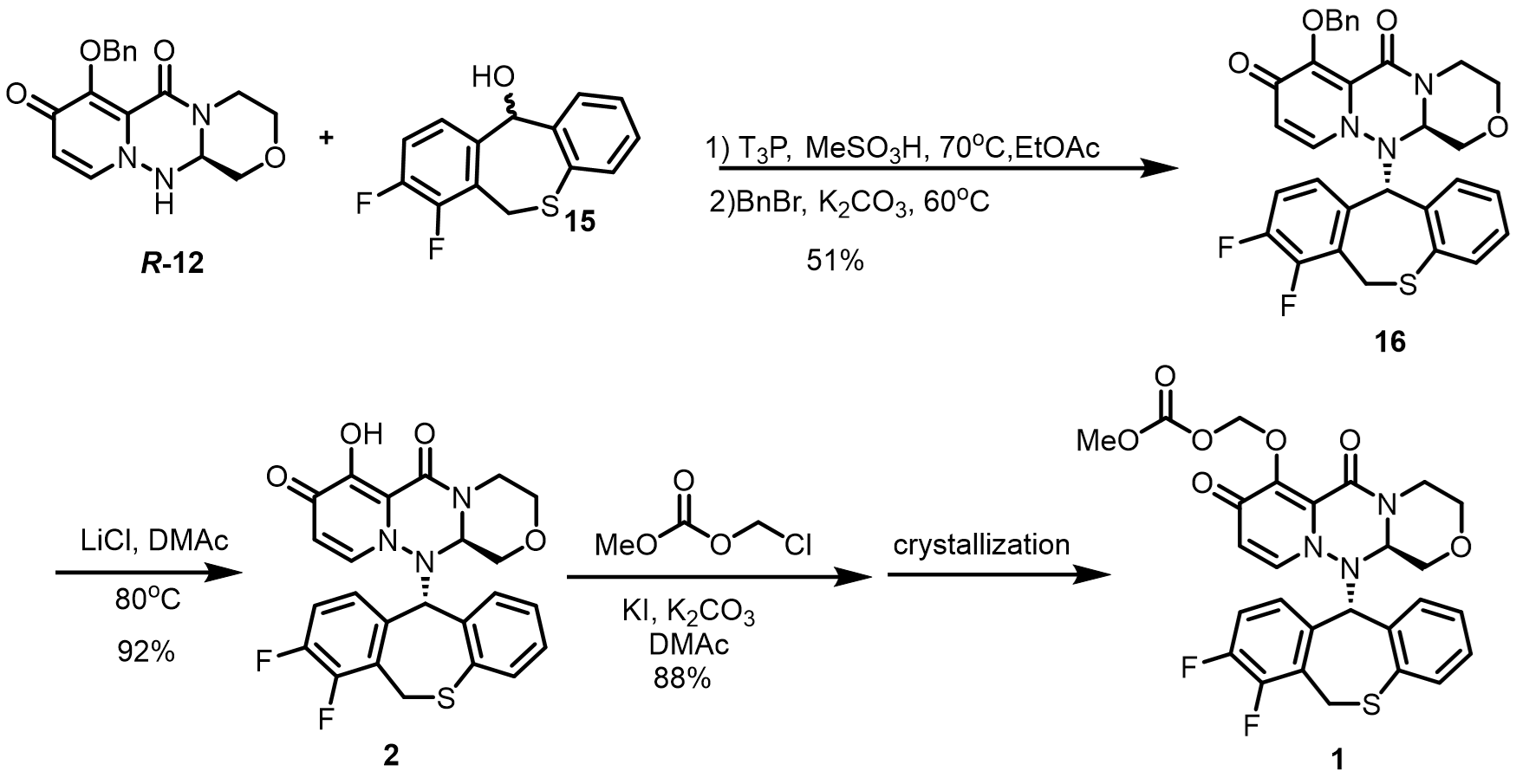
图 7 CMC的放大合成
千克规模(6.74 kg)合成BXM(1)的工艺,如图 7。以R–12和15为原料,经偶联、脱保护以及取代反应,三步以41.3%的总产率获得BXM。
结束语
玛巴洛沙韦的现有合成路线标志着抗流感药物合成领域的一项重大进步。从最初的实验室探索到如今的工业化生产,其合成工艺在原子经济性、步骤收敛性和环境友好性方面不断优化。本文主要描述了三嗪酮R–12及中间体16的千克规模工艺的发展和优化。此外,三嗪酮R-12和15作为原料,经过偶联、脱保护以及取代反应,三步以41.3%的总产率获得一期临床的BXM。
参考资料
Anan, K., Miyagawa, M., Okano, A., Sugimoto, H., Miyake, N., Fukui, N., Kijima, A., Tanimoto, E., & Kawai, M., First-Generation Process Development for the Synthesis of Baloxavir Marboxil: Early-Stage Development of Synthetic Methods to Prepare Baloxavir Marboxil Intermediates. Org. Process Res. Dev. 2024, 28, 2117–2127. DOI: 10.1021/acs.oprd.3c00514
推荐阅读
- 杂质谱
Huixiong Lu, Guobin Xu, Jingping Kou, Shuming Wu, Jiebin Zeng, Yuting Liu, Jidi Lin, Yongbo Xu, Wei Shang, Yaoyao Li, and Zhongqing Wang. Identification, Synthesis, Characterization, and Control Strategy Establishment for Process Impurities of Baloxavir Marboxil, Org. Process Res. Dev., 2024, 28 1170-1185. DOI: 10.1021/acs.oprd.4c00011
- 连续流工艺
- Hannah Nguyen, Wei Wu, Rita C. Barral, Rajshree Chakrabarti, Qinglin Su, Youhua Li, Anjana Ramnath, Bhavya Singh, Ke Wen, Yazid Al Khatib, Khrystyna Shvedova, Stephen C. Born, Chuntian Hu, Bayan Takizawa, Paul Stonestreet, Michael Berg, and Salvatore Mascia. Process Development for Continuous Manufacturing of Baloxavir Marboxil. Part 1: Step 1 Synthesis., Process Res. Dev.2025, 29, 1857–1868. DOI: 10.1021/acs.oprd.5c00156.
- Rita C. Barral, Hannah Nguyen, Rajshree Chakrabarti, Bhavya Singh, Wei Wu, Shalabh S. Yeole, Youhua Li, Anjana Ramnath, Uma Raul, Aibolat Koishybay, Taryn Sparacino, Michael Stamm, Chuntian Hu, Bayan Takizawa, Paul Stonestreet, Michael Berg, and Salvatore Mascia, Process Development for Continuous Manufacturing of Baloxavir Marboxil. Part 2: Step 2 Synthesis., Process Res. Dev.2025, 7, 1843–1856. DOI: 10.1021/acs.oprd.5c00157
- 晶型研究
Hongshuai Wang, Lei Wang, Guanying Xie, Changlin Yao, Shuhong Song, Huimin Li, Yaqian Qu, Peizhuo Han, Zeliang Gao, and Xutang Tao, Solvates and Polymorphs of Baloxavir Marboxil: Crystal Structure and Phase Transformation Study, Cryst. Growth Des. 2024, 24, 3399–3409. DOI: 10.1021/acs.cgd.4c00120





















No comments yet.