自由基聚合反应(free radical polymerization),为用自由基引发,高活性的中性自由基种作为链增长的聚合反应。这一方法,因为可在水中进行、低消耗而在工业界广泛应用。但是,通常的自由基聚合反应会有两种链终止反应:
- 两个链增长自由基的结合会使得自由基活性种消失,聚合反应终止–双基终止[图1 (1)];
- 反应中单侧的链增长自由夺取氢原子,会生成饱和端基与不饱和端基的两个高分子的非均一反应[图1 (2)]。
有这两种终止反应存在,导致聚合物增长停止,产物分子量不均一。(图 1) 聚合物的分子量分布与其物化性质有着很大关系,化学家们一直在寻求开发能生成均一分子量分布的聚合反应。
原子转移自由基聚合(Atom Transfer Radical Polymerization)
为了解决上述的问题点,1995年, Matyjaszewski、王锦山、澤本(Sawamoto) 等人提出了原子转移自由基聚合反应(ATRP)[1]。该方法是金属卤化物与有机卤化物作为自由基引发剂,活性种Pn・可以和引发剂的卤素结合成为休眠种Pn-X,从而在休眠种和活性种之间建立一个可逆平衡。这样一来,体系中的活性种的浓度会降低,链终止副反应会得到抑制,通过这种方法使得合成长链,分子量分布均一的聚合物成为可能。[4](图 2)。 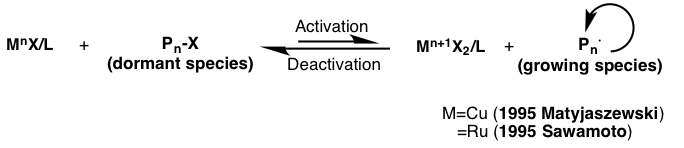
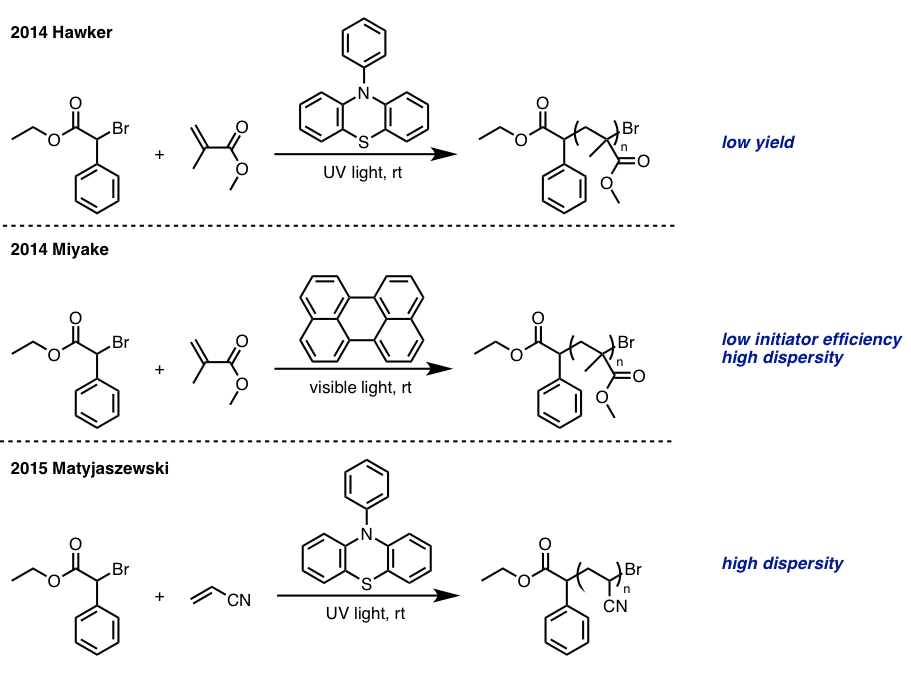
以往的ATRP法中都使用金属催化剂,而生成的高分子聚合物在电子材料、生物医药中使用时,通常残留金属杂质会影响其性能。因此,近年来,利用有机光催化剂代替金属催化剂的O-ATRP法已经得到广泛的关注和研究。理想型聚合物合成方法必须是分子量分布均一、具有高聚合度并且较好收率这些必要因素,除此之外,自由控制分子量的聚合物合成方法也是化学家们希望突破实现的。目前为止发现的O-ATRP有三例研究,但能全部满足以上要求的还没有被报道过。(图 3)[5]。
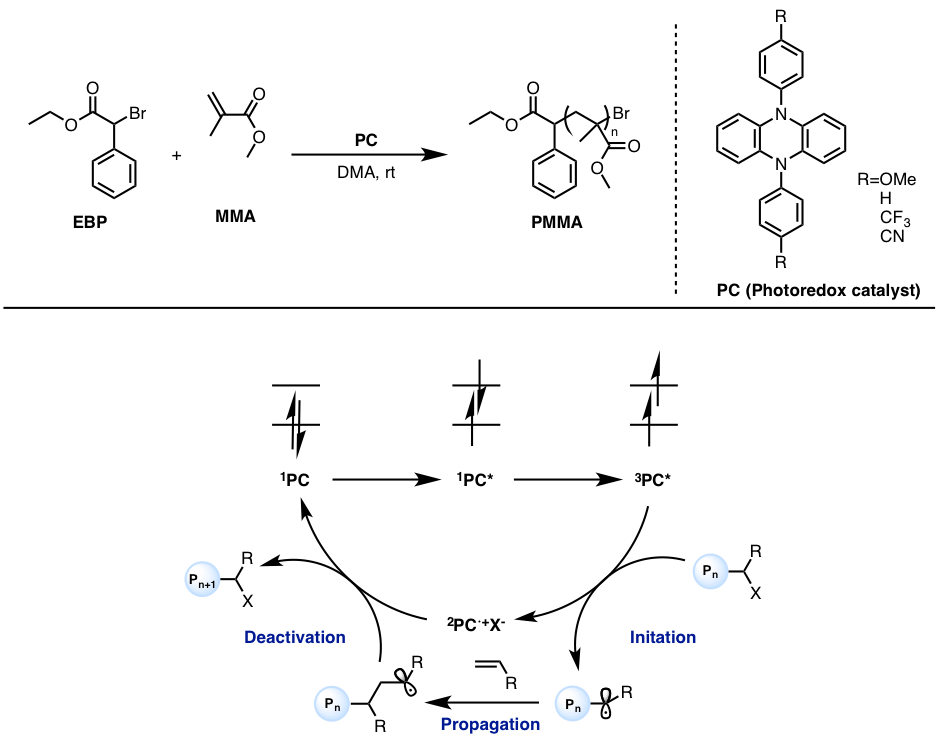
最近,美国科罗拉多大学波尔德分校的Miyake等人,利用5,10-二苯基-5,10-二氢吩嗪衍生物作为有机光催化剂,在可见光照射、室温下成功合成了多分散系数 D = 1.1 (分子量变化非常小)的高分子聚合物,该研究被刊登在Science杂志中。
“Organocatalyzed atom transfer radical polymerization driven by visible light”
Theriot, J. C.; Lim, C.-H.; Yang, H.; Ryan, M. D.; Musgrave, C. B.; Miyake, G. M. Science 2016, 352, 1082. DOI: 10.1126/science.aaf3935
利用有机光催化的自由基聚合反应的反应机理
该反应的机理如下图4所示。
- 通过可见过照射,有机光催化剂激发到单线态激发态(1PC*),接着经历隙间穿越(ISC)变为三线态激发态(3PC*);
- 3PC*与休眠种发生单电子转移,转化为自由阳离子基(2PC・+),同时被还原的休眠种变为活性种,链增长反应开始;
- 活性种与有机光触媒之间发生单电子转移使得光催化剂再生,同时,被氧化的活性种再变为休眠种,使得链增长停止。
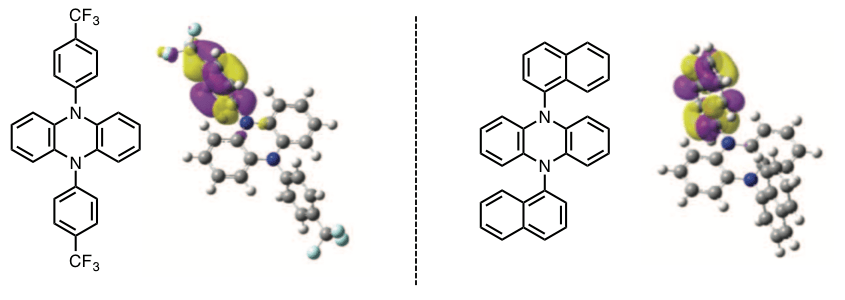
该催化反应体系中,可见光照射一旦停止,聚合物链增长也会随之立即停止,于此同时,分离所得聚合物中加入不同底物,有机光催化剂存在下用可见光照射,成功实现一个聚合物中含有两种链的嵌段聚合物。在5,10-二苯基-5,10-二氢吩嗪衍生物中,尤其是对高催化活性的三氟甲基取代苯基衍生物计算其三线态3PC*的high-SOMO分子轨道时,发现单侧的苯基及三氟甲基上的电子发生离域共轭(图 5,左)。遵循这一计算结果,设计在3PC*的high-SOMO状态下单侧取代基上的电子离域状态的催化剂,并用于反应中,高收率的成功合成了多分散系数 D = 1.28,数均分子量与理论值非常接近的聚合物。另外,可通过改变引发剂或者单体的当量来成功制御合成任意分子量的聚合物。(图5,右)。
总结
这一研究中,Miyake等人,通过有机光催化剂在可见光照射下,成功合成了分子量差别较小,数均分子量与理论值很接近的聚合物。本反应条件温和而且不使用金属催化剂,可以说是一种新型实用的反应,可应用于在聚合物材料合成中。另外,该反应也成功合成了共嵌聚合物,期待今后能够作为一种有效合成方法应用于聚合物的多样性合成中。
参考文献
- 聚合物的分子量变化程度一般用多分散系数D表示,D值越接近1,就说分子量变化越小,聚合物均一性越高。
- (a) Wang, J.; Matyjaszewski, K. J. Am. Chem. Soc. 1995, 117, 5614. DOI: 10.1021/ja00125a035(b) Kato, M.; Kamigaito, M.; Sawamoto, M.; Higashimura, T. Macromolecules 1995, 28, 1721. DOI: 10.1021/ma00109a056
- Matyjaszewski, K. ACS Symposium Ser. 2015, 1187, 1.
- (a) Treat, N. J. et al. J. Am. Chem. Soc. 2014, 136, 16096. DOI: 10.1021/ja510389m (b) Miyake, G. M.; Theriot, J. C. Macromolecules 2014, 47, 8255. DOI: 10.1021/ma502044f (c) Pan, X.; Lamson, M.; Yan, J.; Matyjaszewski, K. ACS Macro Lett. 2015, 4, 192. DOI: 10.1021/mz500834g
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!


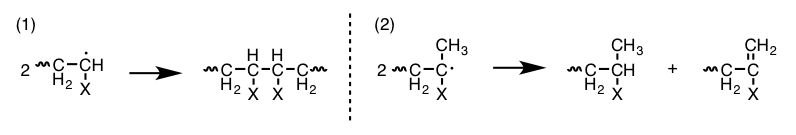














No comments yet.