以往,我们都是用改变底物、催化剂、反应条件等等一系列因素来分析检测反应「収率的変化」来开发新反应,不过这一次为大家介绍的论文,提出了通过追踪观察「反应中间体」作为一种新型手法来开发反应。
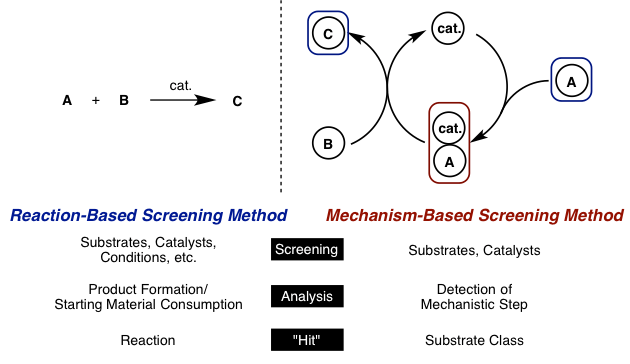
开发反应时,一般都是对底物的消耗量、生成物的追踪比如对底物、催化剂、反应条件的改变来筛选反应(Reaction-Based Screening)。
最近,由德国明斯特大学Glorious教授等人报道的Mechanism-Based Screening不是对影响反应的所有因素,只针对预想的催化循环的一部分进行调查研究,以此作为发现新反应的有效方法。这一次就给大家八一八这个方法的具体实践研究。
“Accelerated Discovery in Photocatalysis using a Mechanism-Based Screening Method”
Hopkinson, M. N.; Gómez Suárez, A.; Teders, M.; Sahoo, B.; Glorius, F.; Angew. Chem. Int. Ed. 2016, 55, 4361. DOI: 10.1002/anie.201600995
MECHANISM-BASED SCREENING的Concept
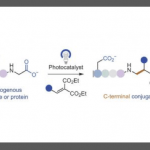
例如对化合物A用催化剂活化后,与B作用后生成C的反应(如下图1)。用这一新方法的话是对催化剂和化合物A作用生成的中间体的分析检测,来高效确定反应适合的底物范围。
MECHANISM-BASED SCREENING的步骤
研究者们对上述设想通过在新型光催化反应的开发中来实践验证,光催化剂在光照下变激发态,催化剂与底物之间通过单电子转移形成氧化/还原活性种(中间体)[1]。通过荧光光谱观测催化剂活化底物的过程,通过荧光光谱的强度只含催化剂的溶液(I0)和催化剂底物都有的溶液(I)由下面的公式算出Quench率(F)。
筛选1. Quencher discovery、2. Quenching evaluation这两个阶段分步来进行。
1.Quencher discovery
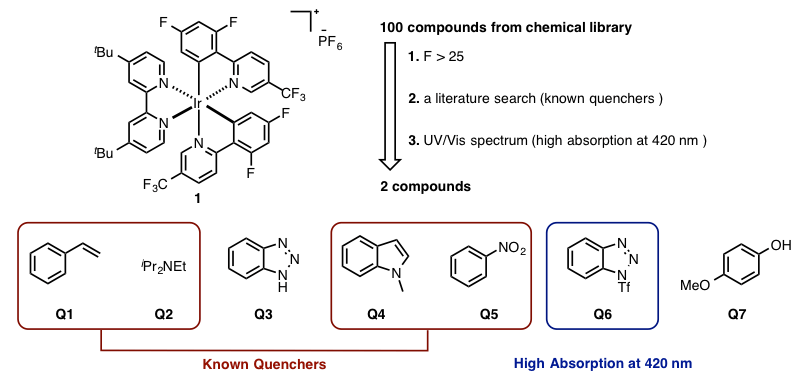
催化剂是光催化反应频繁使用的铱络合物:使用[Ir(dF(CF3)ppy)2(dtbbpy)]PF6 (1)[2]、并从化合物libary库群随即选中100种化合物进行筛选(图 2)。F>25的化合物则被选中,由此得到7个化合物(Q1–Q7)。
从这其中,因为研究者们是想开发新型反应,所以Quencher排除了其中4种化合物。
剩下的3个化合物(Q3, Q6, Q7),通过紫外可见吸收光谱的测定得知,Q6在铱络合物1的最大激发波的波长(420 nm)处有很高的吸收。也就是说通过Quencher,得知不是荧光强度的变化,而是由于Q6对激发光的吸收使得F值变高。因此Q6也被排除,最终新型Quencher候选化合物为Q3和Q7两个。
2. Quenching evaluation
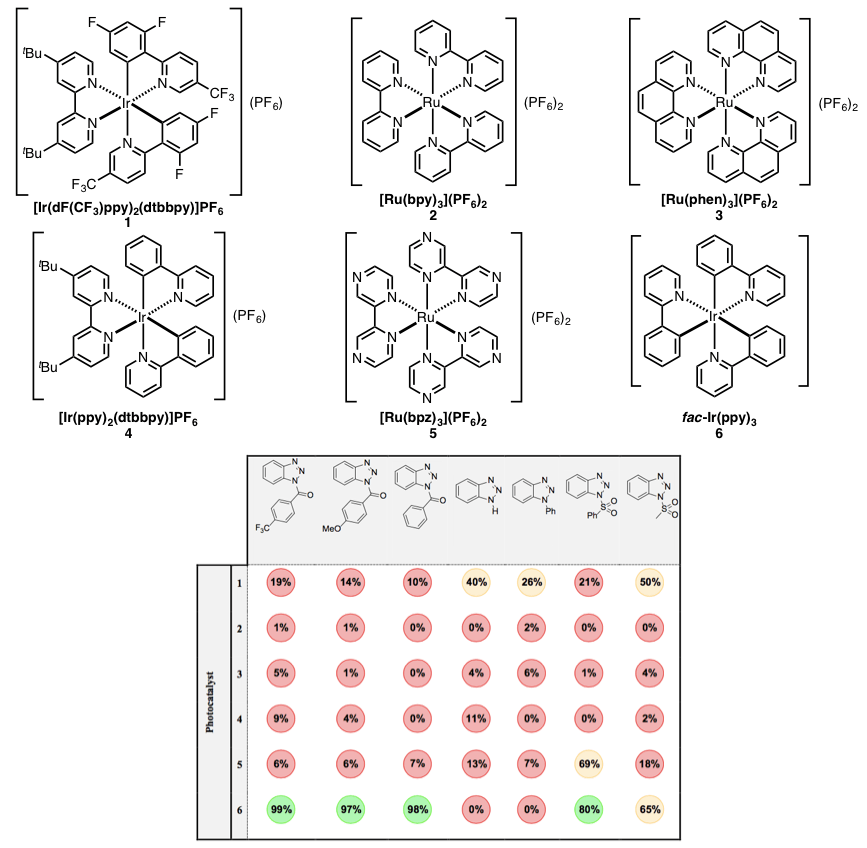
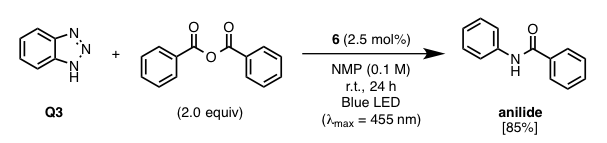
接下来研究者们对上述的苯并三唑Q3以及它的衍生物,通过铱络合物1以外的几种光催化剂作用来继续筛选优化(图 3)。只有当苯并三唑的N上含有吸电子、用铱催化剂6的条件下,才获得较高的F值。
同时,研究者们推测,由于铱催化剂6的有较高的氧化电位,N上的吸电子基是的苯并三唑的还原电位降低,这样通过苯并三唑的单电子转移而使反应进行。通过单电子还原使得三唑的部位发生开环,生成重氮盐,接着通过脱氮及自由基负离子的氢化生成胺[3]。通过优化条件,他们发现Q3与催化剂6,在NMP溶剂中通过光照与无水安息香酸作用,能够高收率的得到胺(图4)。
小结
这一次Glorious等人是着眼于反应机理,开发新的反应Screening方法,并由此成功发现新型光催化反应。该Screening方法只需重点分析反应中生成的一种中间体,便能迅速确定催化剂和底物的最佳组合。反应条件的所有的最佳因素决定必须经过Reaction-Based Screening。与通常的方法相比,该反应能发现反应物和催化剂的组合,因此发现新反应更加高效快捷。
参考文献・链接
- 可见光氧化还原催化剂
- Lowry, M. S.; Goldsmith, J. I.; Slinker, J. D.; Rohl, R.; Pascal, R. A., Jr.; Malliaras, G. G.; Bernhard, S. Chem. Mater. 2005, 17, 5712. DOI: 10.1021/cm051312
- Katritzky, A. R.; Ji, F.-B.; Fan, W.-Q.; Gallos, J. K.; Greenhill, J. V.; King, R. W. J. Org. Chem. 1992, 57, 190. DOI: 10.1021/jo00027a036
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载



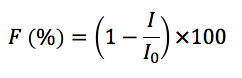






















No comments yet.