概要
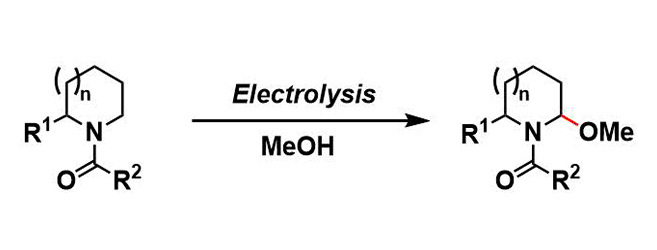
在醇溶剂中电解氧化酰胺或氨基甲酸酯以获得N,O-缩醛的反应。 它可用作胺α位的官能化。
基本文献
- Shono, T.; Hamaguichi, H.; Matsumura, Y. J. Am. Chem. Soc. 1975, 97, 4264. DOI: 10.1021/ja00848a020
- Shono, T.; Matsumura, Y.; Tsubata, K. Tetrahedron Lett. 1981, 22, 3249. doi:10.1016/S0040-4039(01)81876-1
- Shono, T.; Matsumura, Y.; Tsubata, K. J. Am. Chem. Soc. 1981, 103, 1172. DOI: 10.1021/ja00395a029
- Shono, T.; Matsumura, Y.; Tsubata, K. Org. Synth. 1984, 63, 206. DOI: 10.15227/orgsyn.063.0206
- Shono, T.; Matsumura, Y.; Uchida, K.; Tsubata, K.; Makino, A. J. Org. Chem. 1984, 49, 300. DOI: 10.1021/jo00176a016
- Shono, T.; Matsumura, Y.; Tsubata, K.; Uchida, K.; Kanazawa, T.; Tasuda, K. J. Org. Chem. 1984, 49, 3711. DOI: 10.1021/jo00194a008
- Alfonso-Súarez, P.; Kolliopoulos, A. V.; Smith, J. P. Banks, C. E.; Jones, A. M. Tetrahedron Lett. 2015, 56, 6863. doi:10.1016/j.tetlet.2015.10.090
Review
- Shono, T. Tetrahedron 1984, 40, 811. doi:10.1016/S0040-4020(01)91472-3
- Onomura, O. Heterocycles 2012, 85, 2111. DOI: 10.3987/REV-12-744
- Jones, A. M.; Banks, C. E. Beilstein J. Org. Chem. 2014, 10, 3056. doi: 10.3762/bjoc.10.323
发展史
京都大学的庄野達哉开发的反应。
反应机理
形成N-酰基亚胺离子中间体,并且反应以以溶剂醇捕获的形式进行。当用低温/非醇溶剂进行电解时、N-酰基亚胺中间体进行汇聚、并且可以与醇以外的亲核试剂直接反应。(阳离子池法)。
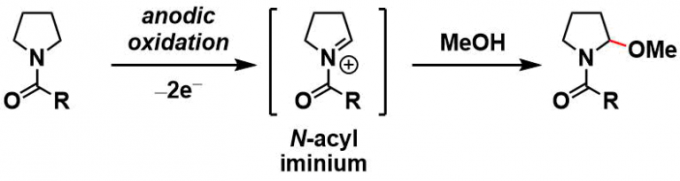
反应实例
在有机电解反应中,有许多研究实例,并且常应用于复杂化合物的合成。
产物N,O-缩醛可用于形成新的C-C键形成。下面是一个进行托烷骨架合成的例子[1]。
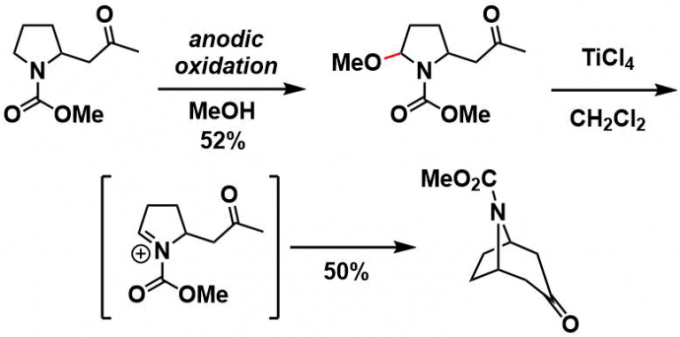
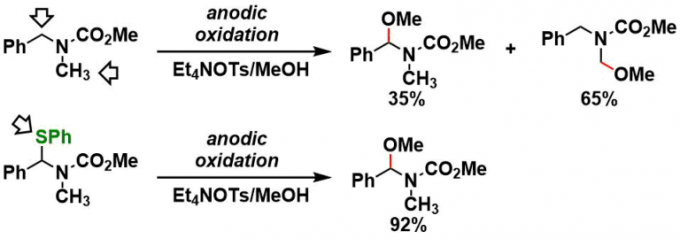
对于如下图所示的两侧非对称的底物来说,位阻小的一侧通常更容易被氧化,然而当N-氰基取代的时候,选择性发生逆转[2]。此外,对于双环氨基甲酸酯底物,会发生多取代反应[3]。
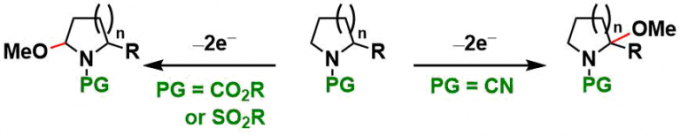
阳离子池法进行的庄野氧化→亲核加成[4]
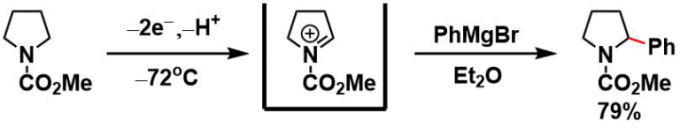
使用电解辅助基(electroauxiliary)的位置选择性的氧化[5]:下面的例子就是SPh基团作为电解辅助基团,调节氧化的区域选择性。同样TMS也能经常用于达到同样的目的。
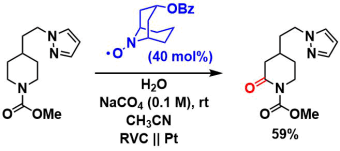
使用电解质的庄野氧化[6]:官能团的兼容性高是该反应的特征。
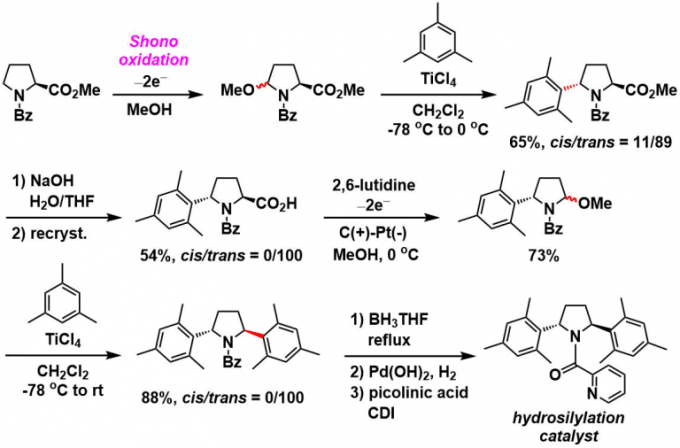
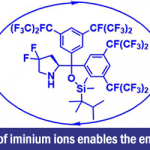
光学活性二芳基吡咯烷的合成[7]:用于合成手性氢化硅烷化催化剂的bulding block。
参考文献
- Shono, T.; Matsumura, Y.; Tsubata, K. J. Am. Chem. Soc. 1981, 103, 1172. doi:10.1021/ja00395a029
- Libendi, S. S.; Demizu, Y.; Matsumura, Y.; Onomura, O. Tetrahedron 2008, 64, 3935. doi:10.1016/j.tet.2008.02.060
- Onomura, O.; Ishida, Y.; Maki, T.; Minato, D.; Demizu, Y.; Matsumura, Y. Electrochemistry 2006, 74, 645.
- Suga, S.; Okajima, M.; Yoshida, J.-i. Tetrahedron Lett. 2001, 42, 2173. doi:10.1016/S0040-4039(01)00128-9
- Sugawara, M.; Mori, K.; Yoshida, J.-i. Electrochim. Acta 1997, 42, 1995. doi:10.1016/S0013-4686(97)85473-4
- Wang, F.; Rafiee, M.; Stahl, S. S. Angew. Chem. Int. Ed. 2018, 57, 6686. doi:10.1002/anie.201803539
- Onomura, O.; Kirira, P. G.; Tanaka, T.; Tsukada, S.; Matsumura, Y.; Demizu, Y. Tetrahedron 2008, 64, 7498. doi:10.1016/j.tet.2008.06.004
外部链接
- Electroorganic chemistry(PDF, Baran’s lab)
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.