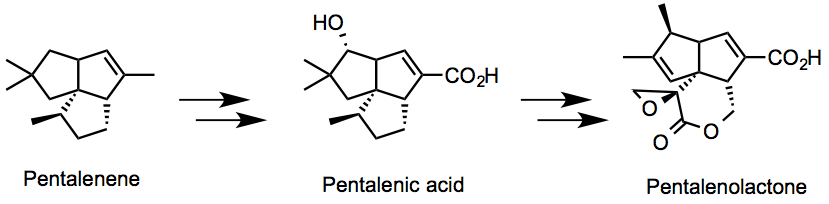
并环萜烯(Pentalenene)是由多种放线菌(Streptomyces chromofuscus, S. griseochromogenes, S. baarnensis)产生的倍半萜类化合物。并环萜烯是针对革兰氏阳性菌、阴性菌、霉菌等具有抗生活性的抗生物质–戊丙酯菌素(Pentalenolactone)的生物合成中间体,并环萜烯1980年由瀬戸治男成功分离得到。(文献1)。从生物合成的观点来看,关于这一特征的三并五元环骨架(triquinane structure)是如何形成的,已经展开了许多研究。(多个并五元环结构单元被称为polyquinane类化合物、因环的数目不同分为diquinane、triquinane等。)
并环萜烯的生物合成
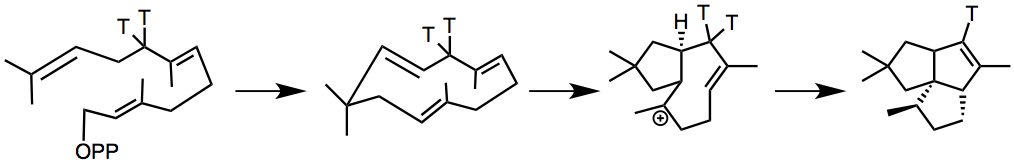
天然产物界权威化学家David Cane一直致力于并环帖烯的生物合成研究。Cane等人是1983年从放线菌提取物中加入氚标记的FPP,追踪其生物合成机理(文献2)。所得结果,见下图,由此得知该合成是通过FPP酶环化得到并环萜烯。
并环帖烯的合成酶的分离、解析
接着Cane等人在1994年将并环帖烯的合成酶成功分离纯化,明确其序列信息(文献4),由此,可以利用大肠杆菌发现其变异体,从而完成了酶的高效测定。
2002年,人们成功结晶得到并环帖烯合成酶,经由氨基酸变异实验等研究详细得到该反应的机理。
并环帖烯的生物合成机理的理论计算
2006年,由Dean Tantillo等人通过DFT计算了帖烯的的生物合成相关反应机理。
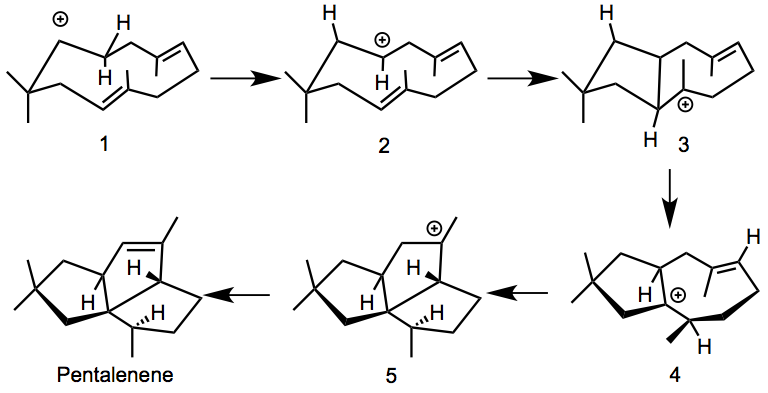
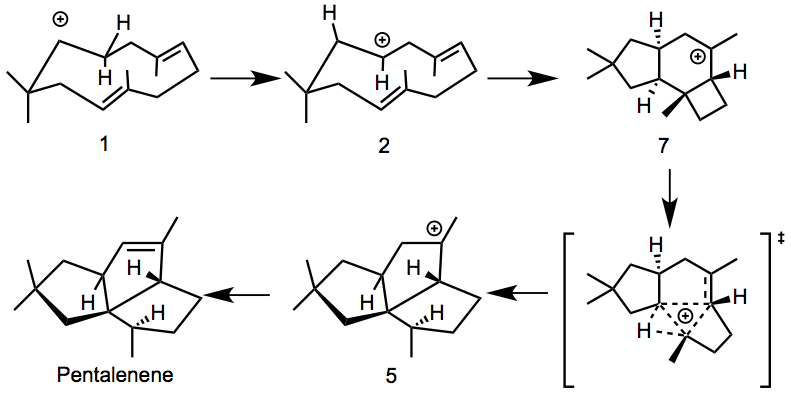
帖烯的生物合成反应机理最初的设想见下图。
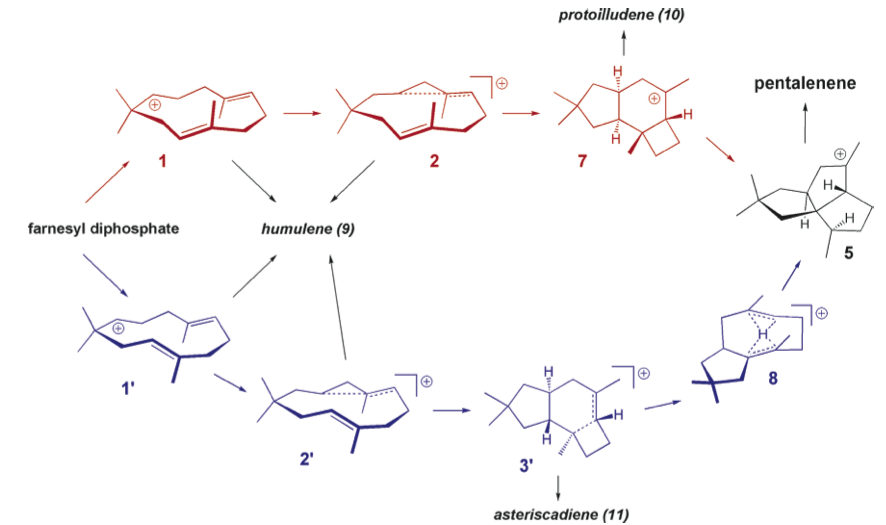
而通过DFT计算得到的反应机理,则如下所示。人们最初设想的化合物3不是local minimum,明确了它并不是反应中间体。取而代之,人们发现具有5-6-4元环结构的化合物7,才是反应中的中间体。
另外,酶环化反应还得到另一构象1’,由此得到另一条路线:该反应过程中,当两个烯烃将质子束缚会形成三明治结构过渡态中间体(8)。
两者的路线在triquinane的骨架形成时都需要近30 kcal/mol的能量,所以估计在室温条件下反应会比较慢。不过,具体需要多少 kcal/mol才能反应也没有一个严格的标准,另外,Tantillo等人得出结论,关于这一过渡态的稳定化很大程度上与环帖烯合成酶有关。
总结
并环帖烯的生物合成,经历了30年以上。Cane在1980年代的研究中,因为无法分离得到酶,将放线菌的提取液作为底物投入使用;进入1990年代后,酶的分离、纯化、遗传序列的确定、变异体的发现都成为可能;再后来,2000年以后,酶的成功结晶化,以及关于其活性部位的研究都可以进行了;直到2006年,Dean Tantillo借助计算化学,详细的阐明了其反应机理。追踪这个研究的进程就能够实实在在感受到科学技术的进步。
参考文献
- Haruo Seto, et al. J. Antibiot. 1980, 33, 92-93.
- Cane, D. E. et al. J. am. chem. soc. 1983, 105, 122-124. DOI: 10.1021/ja00339a026
- David E. Cane. et al. J. am. chem. soc. 1990, 112, 4513-4524. DOI: 10.1021/ja00167a059
- David E. Cane. et al. Biochemistry 1994, 33, 5846-5857. DOI: 10.1021/bi00185a024
- David E. Cane. et al. J. am. chem. soc. 2002, 124, 7681-7689. DOI:10.1021/ja026058q
- Pradeep Gutta and Dean J. Tantillo, J. am. chem. soc. 2006, 128, 6172-6179. DOI: 10.1021/ja058031n
- Y.-J. Kim et al., Tetrahedron 2013 69, 7810-7816. DOI: 10.1016/j.tet.2013.05.095
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
















No comments yet.