一、个人简介
谭斌(课题组主页),南方科技大学终身正教授,化学系副主任、博士生导师。本科和硕士分别毕业于湖南科技大学和厦门大学,2010年博士毕业于新加坡南洋理工大学化学与生物化学系,师从钟国富教授,研究方向为新型手性有机催化剂的设计及不对称多米诺反应的研究。博士后期间,谭斌在有机小分子催化领域的发源地——美国Scripps研究所师从Barbas教授,继续从事催化不对称催化合成的研究。2012年9月,谭斌以准聘(Tenure-Track)副教授身份加入南方科技大学化学系。2018年1月晋升为终身正教授,目前担任《中国科学-化学》和《中国化学》青年编委。
二、荣誉和奖励
- 2019年,南方科技大学卓越科研奖
- 2019年,国家科技部创新人才推进计划“中青年科技创新领军人才”
- 2018年,深圳市鹏城学者“特聘教授”
- 2017年,2017中国新锐科技人物(知社学术圈)
- 2017年,Asian Core Program Lectureship Award (日本)
- 2016年,南方科技大学杰出科研奖
- 2016年,Asian Core Program Lectureship Award (新加坡)
- 2013年,深圳市海外高层次人才“孔雀计划”B类入选者
三、研究领域
2012年9月,谭斌教授回国后加盟南方科技大学化学系,主要从事轴手性化学、多组分反应、芳基官能团化以及靶向分子的合成等方面的研究。目前为止,谭斌教授已经在国际高水平期刊发表论文60余篇,这些原创成果极大推动了国内外相关领域的研究热潮。
(1)轴手性分子的构建与应用
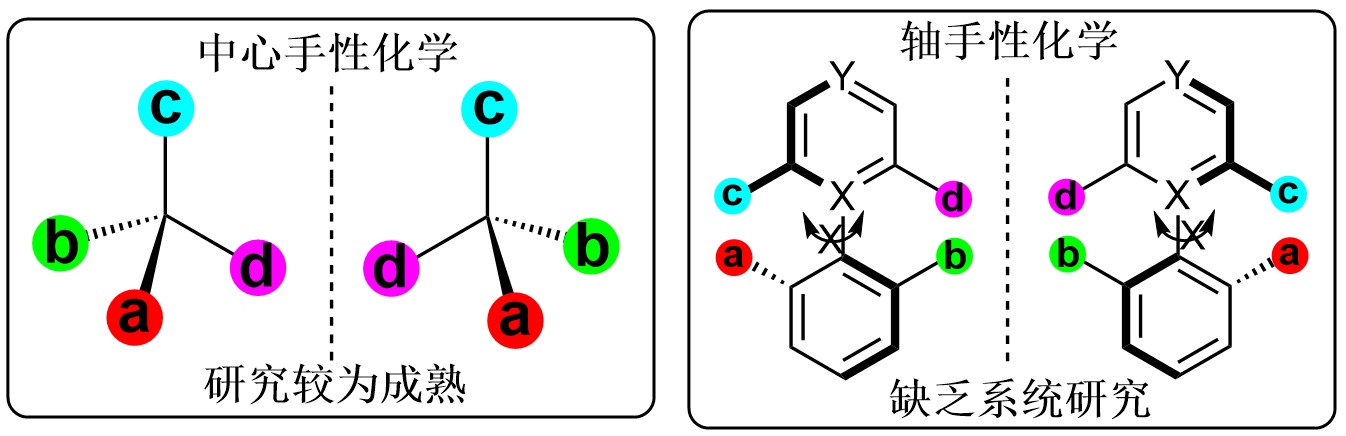
手性(chirality)是自然界的基本属性,手性化合物与人类的生活息息相关,在人类健康、生命科学、材料科学以及环境科学等领域有着广泛用途。需要指出的是,目前有超过半数的临床药物是手性药物,著名的“反应停”事件也让人们意识到获得手性纯药物具有重要意义。过去的几十年里,不对称催化一直是高效获得手性化合物的重要方法。
关于手性物质的研究,目前大都集中于中心手性,并且过渡金属催化、有机小分子催化和生物催化几乎占据了整个不对称催化领域。然而,目前对于轴手性化合物的研究却非常有限,所谓轴手性是指分子中由于化学键不能自由旋转导致对映异构体的产生,例如目前被广泛使用的手性配体BINOL、BINAP、BINAM等。
图片来源于谭斌课题组主页
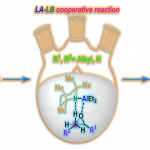
近年来,谭斌教授在有机催化构建轴手性化合物领域取得了一系列的原创研究成果,例如利用双酸催化策略,通过简单1,4-二羰基化合物与芳胺发生Paal-Knorr反应高效不对称构建轴手性芳基吡咯骨架化合物[1];利用手性Brønsted酸作为催化剂,以简单的邻氨基苯甲酰胺衍生物为原料,实现了结构多样的轴手性3-芳基喹唑啉酮的不对称合成[2];另外,在手性二级胺的催化下实现了1,3-二酮、丙二腈类亲核试剂与2-位取代的苯乙炔醛的反应,首次高效地合成了具有苯乙烯骨架的轴手性化合物[3]。
(2)催化不对称多组分反应的开发
多组分反应(Multicomponent Reactions,MCRs),顾名思义就是多个原料同时参与反应,一步构建复杂结构目标化合物的方法,例如经典的Ugi四组分反应、Passerini三组分反应、Mannich三组分反应等。由于多组分反应具有操作简单和原子利用率高的特点,非常符合绿色化学理念,近些年一直备受合成化学工作者的青睐。
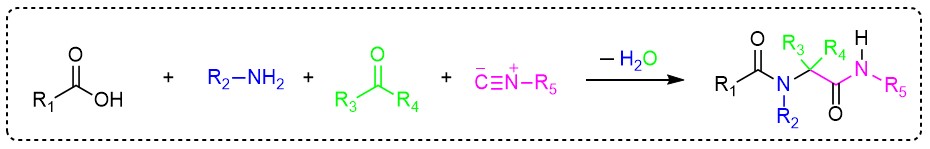
经典的Ugi四组分反应通式
经典的Ugi反应是一分子的羧酸、羰基化合物、胺和异腈脱水缩合得到a-酰氧基酰胺化合物,发现于20世纪60年代,被广泛用于药物合成并且在有机化学领域也占有重要地位。然而,传统的Ugi反应都只能得到消旋体产物并且很难实现其拆分,如何实现不对称Ugi反应是全世界科学家们都在努力克服的挑战。
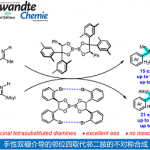
2018年9月,谭斌教授在国际顶级学术期刊《Science》上以长文形式报道了手性磷酸催化的不对称Ugi四组分反应,解决了近60年来合成化学家一直挑战的科学难题[4]。基于手性磷酸被广泛用于亚胺C=N双键活化的报道,考虑到Ugi反应也涉及到亚胺中间体,谭斌教授课题组精心设计了新型手性磷酸催化剂并将其用于亚胺中间体的手性调控,最终以高产率和高立体选择性实现了不对称Ugi反应,同时他们与加州大学洛杉矶分校(UCLA)合作,通过理论计算对反应机理和手性诱导模式进行了详细的阐释,为相关研究提供重要参考。
图片来源于Science, 2018, 361, eaas8707.
(3)芳基的活化与官能团化
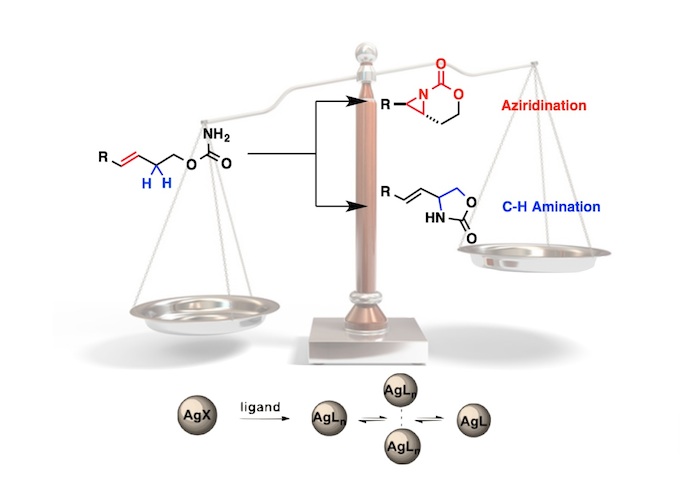
过去的几十年,基于金属催化和导向基协助的碳-氢键活化在芳烃官能化方面取得了深远发展,然而借助有机催化实现的碳-氢键官能团化反应却十分少见。2017年,谭斌教授大胆设想利用偶氮基团同时作为导向和活化基团,借助手性磷酸来实现吲哚的不对称芳基化反应,进而构建轴手性的联芳化合物,相关成果发表于国际顶级期刊《Nature Chemistry》[5]。
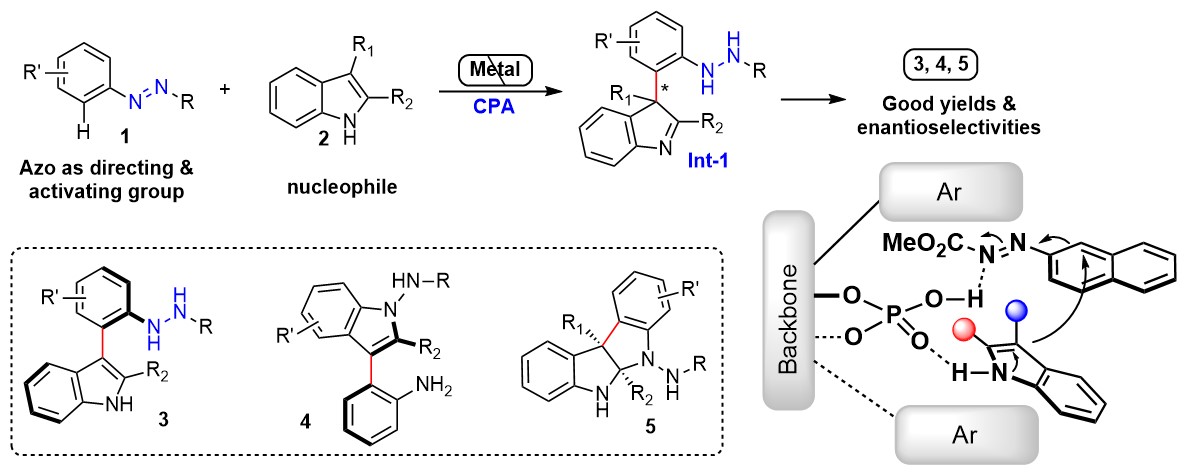
谭斌教授延续以往的工作,以手性磷酸作为有机分子催化剂,通过调控吲哚底物的取代基实现了轴手性的芳基吲哚、邻苯氨基吲哚以及具有两个连续季碳手性中心的吡咯并吲哚啉三类产物的构建,反应具有理想的收率与优秀的对映选择性。偶氮基团作为反应中重要的导向及活化基团可以提高芳香烃的亲电活性,并在催化剂的引导下接受吲哚底物的亲核芳香取代。
图片来源于Nat. Chem., 2018, 10, 58-64
(4)药物、天然产物和生物活性分子的催化不对称合成
芳基喹唑啉酮作为一类重要的化合物广泛存在于天然产物中,并且具有丰富多样的生物学活性。多种情况下芳基喹唑啉酮体现出轴手性特征,还在体内体现出代谢差异性。Eupolyphagin是从中药土鳖虫中分离出来的天然产物,旋光测试表明该天然产物具有手性特征,但并未对其绝对构型进行确证,主要原因是获得手性纯的芳基喹唑啉酮的方法比较局限,因而发展不对称催化合成轴手性芳基喹唑啉酮的方法具有重要意义。
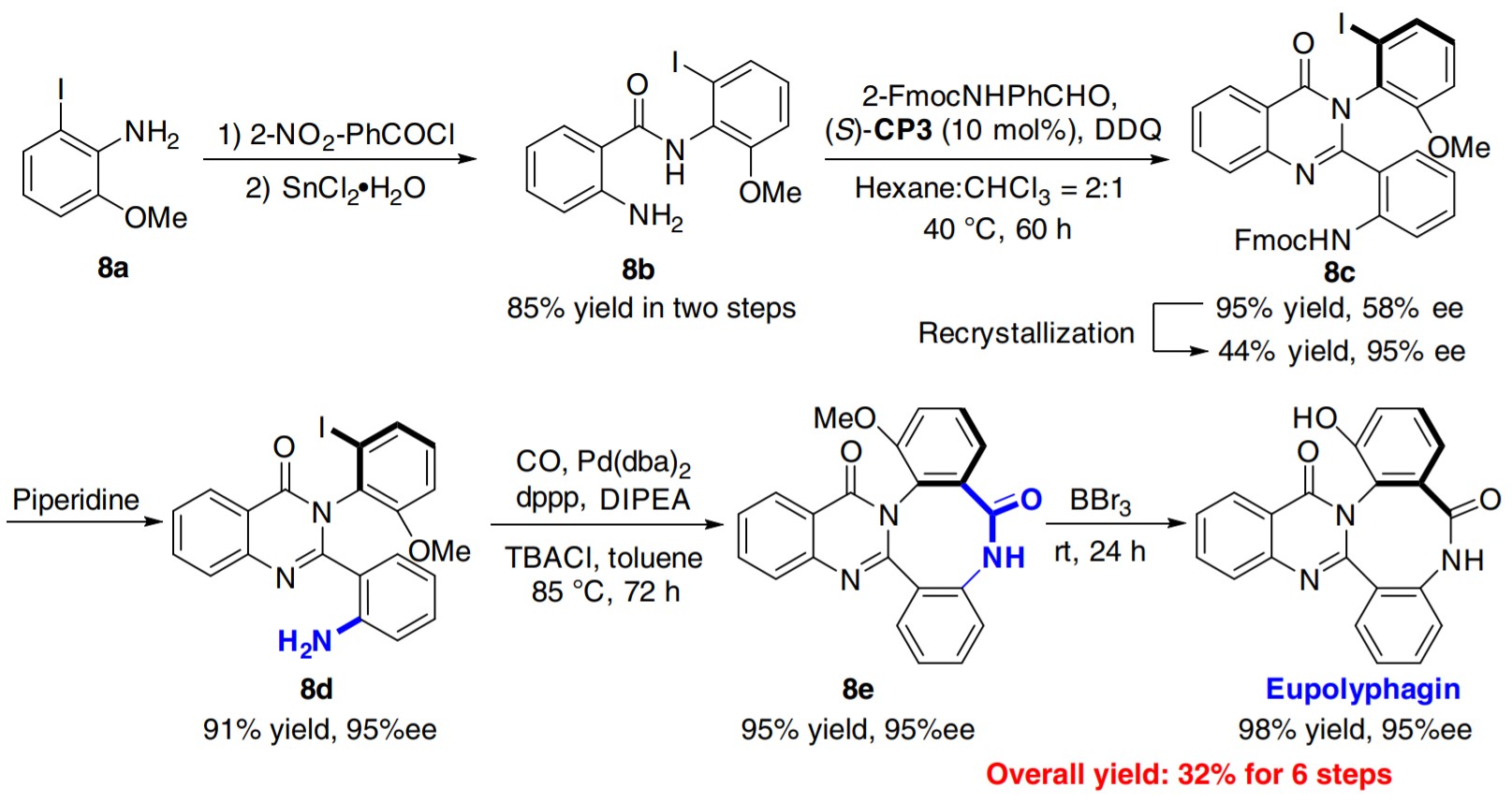
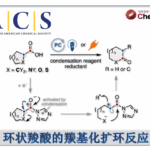
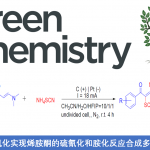
2017年,谭斌教授课题组利用手性Brønsted酸作为催化剂,以简单的邻氨基苯甲酰胺衍生物为原料,实现了结构多样的轴手性3-芳基喹唑啉酮的不对称合成,在此方法的基础上,通过六步反应完成了Eupolyphagin的首次不对称全合成[2]。
图片来源于Nat. Commun., 2017, 8, 15489.
参考文献
- [1] Bin Tan, et al. J. Am. Chem. Soc., 2017, 139, 1714. DOI: 10.1021/jacs.6b09634
- [2] Bin Tan, et al. Nat. Commun., 2017, 8, 15489. DOI: 10.1038/ncomms15489
- [3] Bin Tan, et al. Nat.Commun., 2017, 8, 15238. DOI: 10.1038/ncomms15238
- [4] Bin Tan, et al. Science, 2018, 361, eaas8707. DOI: 10.1126/science.aas8707
- [5] Bin Tan, et al. Nat. Chem., 2018, 10, 58-64. DOI: 10.1038/nchem.2866
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!


























No comments yet.