作者:石油醚
本期热点研究,我们邀请到了本文第一作者、来自德国马克斯·普朗克煤炭研究所(Max-Planck-Institut für Kohlenforschung)的徐睿罡(Ruigang Xu)博士为我们分享。
2026年2月14日,J. Am. Chem. Soc. 在线发表了来自化学诺奖得主Benjamin List教授团队题为「The Catalytic Asymmetric Mukaiyama–Michael Reaction of Silyl Ketene Acetals with Cyclic Enones: Short Routes to Jasmonates」的研究论文。该文中,List团队领衔,报道了一种利用手性硅基Lewis酸催化体系实现的广谱有机催化不对称Mukaiyama–Michael加成反应。该反应针对弱亲电性的环烯酮与烯醇硅醚(enol silanes)或硅基烯酮缩醛(silyl ketene acetals),以高达98%的产率和>99:1的对映体比例(e.r.)高效构建1,4-加成产物,并为下游香料产物茉莉酮酸酯(jasmonates)家族提供了简洁、高效的对映选择性合成路线。
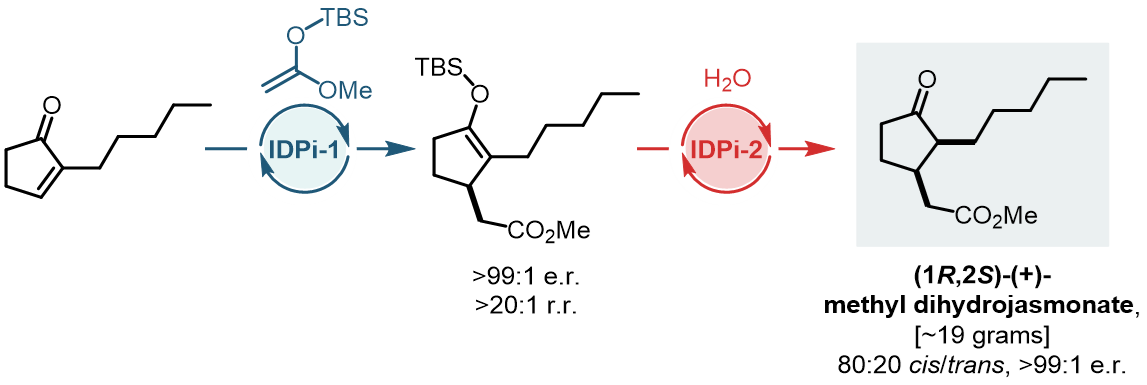
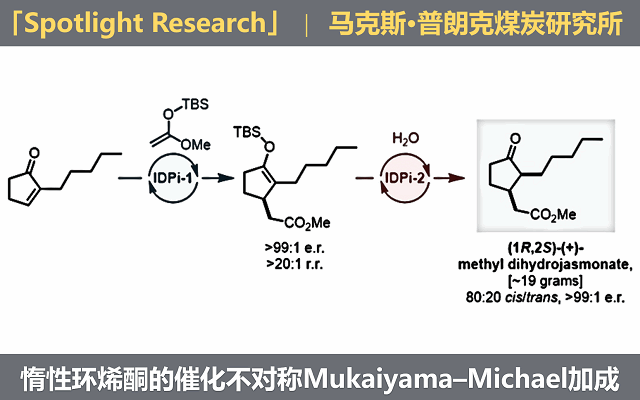
The Catalytic Asymmetric Mukaiyama–Michael Reaction of Silyl Ketene Acetals with Cyclic Enones: Short Routes to Jasmonates
Ruigang Xu, Hui Zhou, Han Yong Bae, Vijay N. Wakchaure, Lorenzo Baldinelli, Isaac F. Leach, Giovanni Bistoni, Philip Kraft, Benjamin List*
J. Am. Chem. Soc. 2026, doi: 10.1021/jacs.5c20804
Q1. 请对‘The Catalytic Asymmetric Mukaiyama–Michael Reaction of Silyl Ketene Acetals with Cyclic Enones: Short Routes to Jasmonates’作一个简单介绍。
过去半个多世纪,Mukaiyama–Michael加成已成为构建C–C键的重要工具,相关不对称版本的研究也取得了显著进展,但迄今为止仍存在两个根本性的科学挑战亟待解决。
其一,环烯酮底物固有的结构刚性以及取代基效应的影响,导致β-位点亲电性显著降低(Poor Mayr Electrophilicity),传统催化体系往往难以同时兼顾高反应活性与高对映选择性,尤其是在α-取代环烯酮体系中这一问题更加突出。
其二,传统金属催化1,4-加成的手性控制通常依赖双齿螯合作用,以增强配位并锚定一个对映选择性的反应面,以实现不对称Mukaiyama–Michael加成的精准控制。然而,对于非螯合、弱配位的亲电底物来说,缺乏能够与催化剂形成强配位或定向相互作用的功能基团,因此对其反应面进行精确手性控制长期以来极具挑战性。
在本研究中,我们开发了一种基于受限空间的硅基Lewis酸催化体系(Si-IDPi),通过构建紧密离子对实现了对环烯酮底物的高效活化与精确立体诱导。该方法适用于硅基烯酮缩醛等亲核试剂,在极低催化剂用量下即可实现高收率和优异的对映选择性,并具有良好的规模化潜力。
同时,我们将该策略应用于珍贵茉莉酮酸酯类香料分子的简洁高效不对称合成,进一步展示了该催化理念在复杂分子合成和特种化学领域的应用前景。
Q2. 有关本次研究的时候遇到过怎样的困难呢?又是怎样克服的呢?
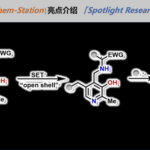
在本研究中,最具挑战性的部分之一来自对映选择性本质的合理解释。硅鎓离子IDPi体系体系涉及高度动态的紧密离子对结构、弱配位相互作用以及显著的色散与溶剂效应,使得反应势能面极为复杂,难以用传统简化模型准确描述。我们尝试了多种分析方法,比如进行了构象空间扫描、steric maps以及静电势分析等,以试图理解IDPi受限空间的手性口袋是如何选择性屏蔽一个反应面。更进一步地,我们采用原子级色散能分解方法(ADLD)定量分析并发现了底物烷基链与催化剂骨架之间存在伦敦色散相互作用(London dispersion),结果显示正是这些弱相互作用对不同催化剂之间的对映选择性差异具有关键贡献,最终帮助我们从微观层面上合理解释了高度对映选择性的来源。
Q3. 本次研究主体,有没有什么让您感觉特别辛苦和烧脑呢?
二氢茉莉酮酸甲酯是dsm-Firmenich等公司非常经典的一款香料原料,其四个立体异构体中, (1R,2S)-(+)-构型具有明亮、通透、令人愉悦的花香,由于其极低的嗅觉阈值(0.015 ng·L–1)与持久的香气,因而在高定线香水配方中备受青睐。
从合成化学角度来看,立体化学的微小差异带来嗅觉上的巨大区别,但也对合成提出了极高要求。在本研究中,我们与德国香料巨头Symrise公司深度合作,希望通过发展不对称Mukaiyama–Michael加成方法,构建茉莉酮酸酯类分子的核心手性骨架,最烧脑且最耗时的部分在于同时控制对映选择性与非对映选择性的控制,特别是后续去硅–质子化步骤以实现下游产品(1R,2S)-(+)-methyl dihydrojasmonate的差向选择性合成。然而产物对体系极其敏感, pKa、溶剂极性、质子源等微小变化都可能导致α-位点消旋。我们系统筛选了多种质子源、溶剂组合,并结合计算模拟优化催化剂结构,最终得到了高达80%顺式比例的(1R,2S)-(+)-methyl dihydrojasmonate,有趣的是,其中20%反式异构体的杂质反而赋予了产品更强烈的茉莉花香和茶香,以及更柔和的柑橘柠檬香和淡淡的果香。这也提示我们在香料开发中,“杂质”有时可能是宝贵的香气贡献者,在未来,我们将进一步深化这类分子的立体选择性合成与香气-结构关系的研究。
Q4. 将来想继续研究化学的哪个方向呢?
基于本阶段的研究工作经验,未来我希望进一步在香料香精化学与特种化学品领域开展研发工作,特别是围绕高附加值香料分子的对映选择性合成方法学与催化策略展开系统探索。目前国际香料产业长期依赖少数跨国公司在核心分子与合成技术方面的创新,而国内在人工合成香料领域的原创性研究仍有较大提升空间。我希望能够将博士阶段的前沿理念引入国内,推动基础研究到工业应用的转化。
Q5. 最后,有什么想对各位读者说的吗?
我想把我的导师Ben List教授经常告诫我们的话,以飨各位同学与年轻科研工作者:
“Trust your own intuition, ideas and follow your enthusiasm(信凭直觉,拥抱灵感,逐梦热情).”
他鼓励我们,无论以后从事哪个行业、哪个方向,哪怕在瞬息万变的世界中,也请始终保持对它们的热爱。尽管追求梦想的路上总是painful与frustrated,但无论如何,兴趣与热情才是真正持久的源动力,它能在最艰难的时刻,给你重新站起来的理由和继续前行的力量。
最后,要特别感谢Chem-Station提供了这样的一个专业平台,让我有机会分享这份研究心得,也欢迎各位同行一起讨论、交流想法。衷心祝愿大家能在自己喜欢的岗位与领域继续发光发热,也希望大家在新的一年科研顺利、成果多多!
作者教育背景简介

教育背景:
2014.09-2018.06 上海电力大学,应用化学,理学学士(导师: 陈文博教授)
2018.09-2021.06 杭州师范大学,化学工程,工学硕士(导师: 钟国富教授)
2021.09-2025.12 Max-Planck-Institut für Kohlenforschung,Chemistry,Doctor of Philosophy(导师: Benjamin List)
本文第一作者徐睿罡师从Benjamin List教授攻读博士学位,以第一作者在JACS, Chem. Commun., Org. Lett.等发表学术论文。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841
请登陆TCI试剂官网查看更多内容
https://www.tcichemicals.com/CN/zh/
















No comments yet.