奋战在研究室第一线的各位有机反应开发研究者们,是不是偶尔也会在过柱子之余抬起头,望着那根可爱无比的柱子,心中默念:我这个反应以后要是能在实际应用派上用场那是真真的好啊。
今天,我们就来说说「新药开发的实际应用中究竟使用了哪些反应?为什么这么反应如此频繁使用?」
本次内容是根据葛兰素史克(GSK)研究所中经常使用的反应为背景,为大家做一个迷你综述。[1]
有哪些反应上位?
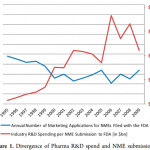
GSK呼吸器系统研究所CEDD(研究所之一)里约有100人是从事合成化学工作的研究者。2005年间这些化学者们共进行了约4800个反应。根据调查显示,这些反应可大致分为以下22组(图1)。
根据结果可以发现,实际上真正常用的反应种类惊人的少。4个反应(烷烃化、缩合反应、利用Pd触媒的交叉偶联反应、保护基)占了该调查全部反应的63%。
此外,有十种反应了占了83%,包括上述四种反应以及卤化反应、杂环生成反应、加水分解、金属化、氧化以及还原。重排反应、自由基反应、烯烃复分解、环化加成反应所占比例都很少。
选择使用反应的条件是?
首先请大家了解的是,上述反应的调查结果多是基于先导化合物探索阶段所用的反应(clinical candidates的寻找阶段)而非化学工艺。基本上所有合成的化合物最后还是要被处理掉,留下初期阶段筛选化验需要的一个检定用量(2mg~6mg),也就是说,只要合成5mg左右的量,足够分析用的就行了。(只有很少数的化合物用于小动物实验或者稍大型一些的动物实验时,需要的检定量系数(-g))
因此,先是要尽可能地多合成一些具有多样性的化合物。随着化合物逐步登上新药的舞台,其多样性也会逐步降低,能拿来合成的化合物种类也随之减少。于此同时,要合成的化合物的量(扩大合成)也会增多(1g-100g)。
一般来说,合成了1000种化合物,最后能用到临床上的少之又少。为什么会这样?笔者试着总结了一下,个人浅见,如有不足之处还请大家多多指教。
理由
①『创药化学的目的是为了尽快地寻找到能在临床上具有实用的化合物,为此,基于方法论上的反应颇为重要。』在追求化合物多样性的初期阶段,需要反应能最大限度地适应反应物底物的不同。
②『底物反应普遍性』这点应该不必多说。例如和苯环相连的苯环上,只想在一个苯环上的一个位置上上官能团的话,大家能想到哪些官能团?Me,Et,iPr,iBu,OH, OMe, CH2OH,F, Cl, NMe2,NHCOR,NHSO2R CO2NH2,CO2H,…这里还没有提到芳香环取代基,就已经有这么多种类了。
顺便提一句,一般情况下我们需要的是各种各样的非共价键结构,或者是为了调整母核的电子云密度、保护容易被代谢掉的位置等,以此作为主要结构框架的考虑基点。
所以说就一个苯环的话也有o,m,p三个取代基上位的不同,可以说化合物的种类巨多。考虑一下资源成本等问题全都合成出来挨个试试也是不可能的。
于是乎,通常情况下我们会设计一个优先顺序。例如、仅限于苯环的话,可利用有名的Topliss Tree [2]手法灵活使用。根据当时的情况,缩小目标,合成基质局部片段,再逐步合成整体。
完成了一元取代分析之后,大家会止步于此吗。当然不会,最少也要试试二元取代物。接下来就是剩下的苯环也用根据以上的思路,从苯环换到复杂些的杂环。还有就是环和环之间的linker也有必要尝试一下各种结构。
总的来说,就算是单纯的芳香环,只要有2个以上,就有必要合成出带有不同物理化学、立体性的取代基的化合物。故而,要使用的反应必须能最大程度的满足底物反应的普遍适用性。
③『官能团的普遍性』。
和上述的②稍有关联,创药化合物中多是带有杂环、酰胺、羟基、胺、羧酸等多种官能团。所以,必然需要运用的反应能够满足当化合物带有以上官能团时也可进行。也就是Buchwald-Hartwig amination, Suzuki-Miyaura cross coupling, Still-Migita-Kosugi cross coupling等等、能满足②、③两项条件的反应。这些反应也是制药界常用的反应。当然,过度依赖这些反应也会带来一些弊端(后述)。
④『创药中对化合物具有的物理性质也是极为重视。特别是化合物有较小的脂溶性(clogP<3)、或者良好的水溶性性质等,这些是在化合物合成上越是到后期越要重视的一点』
这一点如果药物已经合成初具苗头了,再想修正就极为困难。所以在创药研究的初期阶段开始,对这两个参数就要格外注意。分子量较小Hit的话,脂溶性高、又不易溶于水的情况下,要边改善其性质边在增加活性上多下工夫。也就是说,导入极性官能团。这时候Hartwig-Buchwald胺化反应就可以起到作用,图2就是其中一个例子。第一个化合物缺乏脂溶性、第二个化合物脂溶性有所提高,但是水溶性还有待改善。
⑤『增加手性点对手性点安全性的不安』『将新型不对称中心导入Hit to Lead (HtoL)先导化合物时有需要注意避免的地方』
此理由是因为,要说到选择性反应必然会存在对映异构体和非对映异构体。当然,反应的选择性高的话在反应的同时,利用反应速度的差异可以提高纯度的吧。但是,朋友们,任何一点不纯物质的存在,在创药开发上都是棘手的。所有的不纯物质其代谢物、在体内的动态情况、甚至随之而来的副反应问题等,调查这些性质会使工作量增加使研究不得不放慢脚步。
但是,『最近,作为光学活性体的building blocks因为经济优势越来越多的应用于不对称点导入反应中。但是,仍需注意的是,这些不对称点的稳定性』创药的最终阶段是制剂。在原本的化合物中加入添加物,调整生物体内动态。为此,必须要求原化合物在各种环境下(温度/湿度等)要保持光学稳定。此外,进入体内后,要考虑在哪里被代谢。而此代谢是否会导致稳定的不对称中心失去稳定性(外消旋作用),也是必须要加以考证的。
⑥『可购入的催化剂和反应剂以及building blocks』
最重要的一点就是用那些常见市售或者有稳定货源,及时供货的化学品原料,中间体。
⑦『安全性上的疑惑』。
实际上,创药过程中研究者最担心的一个问题就是毒性。上市之后继续进行的跟踪调查就不在话下了,随时随地也都要时刻警惕安全性问题。为此在平时研究过程中就要时刻考虑如何将危险降低到最小限度。不过,至今为止已经知道的带有毒性的官能团,带有此官能团的化合物未必会有毒性。为什么这么说呢,因为这是和官能团的所在的不同位置、立体性、电子环境等决定的。所以稍有经验的创药研究者的话都知道不能一口咬定「那个官能团,它带有毒性不能用于药物中」。只不过,如果知道某官能团具有毒性的可能性很大的话,在有其他可选选项的情况下就没有必要非瞄着这一个官能团去思考了,较危险的官能团如Table1所示。
此篇ref1是一篇较为通俗易懂的文章,有兴趣的朋友们可以读一读。
最后的话
可以说利用钯催化的交叉偶联反应给制药界带来了巨大改革。从底物的一般性反应、官能团耐受性、chemical libary合成,目前大多用在研究初期阶段,而此反应带来的各种问题在2010年之后也陆续出现。
无论如何都要使用交叉偶联反应的话,会倾向于生成平面性较高的化合物。虽然近年来有针对此问题的改善报道,但一般都是在邻位上位阻较大的期待基,而取代基较大会使反应进行困难。
近些年来诺贝尔获奖的有机反应多是因为在实际生产中贡献突出的反应。如果你是瞄着诺贝尔奖的研究者的话,了解制药界大家常关注的一些化合物的话,也许会有些帮助吧!
本篇文章翻译自化学空间日文版,翻译过程中略有改动。原文地址:創薬開発で使用される偏った有機反応
参考文献
[1] Cooper, T.; Campbell, I.; Macdonald, S. Angew. Chem., Int. Ed. 2010, 49, 8082-8091. DOI:10.1002/anie.201002238 [2 ] Topliss Tree:たいていの創薬の基礎の本に記載あり 元文献;Topliss, J. J. Med. Chem. 1972, 15, 1006. DOI: 10.1021/jm00280a002
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!























No comments yet.