作者:杉杉
导读:
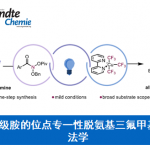
近日,南京大学的郑文华课题组在J. Am. Chem. Soc. 中发表论文,报道一种全新的通过具有C2-对称性的手性硼酸催化剂促进的采用2,2-二取代-1,3-丙二醇参与的催化去对称化反应方法学,进而成功完成一系列具有四级碳立体中心的手性二醇分子的构建。
Synthesis of a C2‑Symmetric Chiral Borinic Acid and Its Application in Catalytic Desymmetrization of 2,2-Disubstituted-1,3-Propanediols
J.Song, W.Zheng, J. Am. Chem. Soc. 2023, 145, 8338. doi: 10.1021/jacs.3c02331.
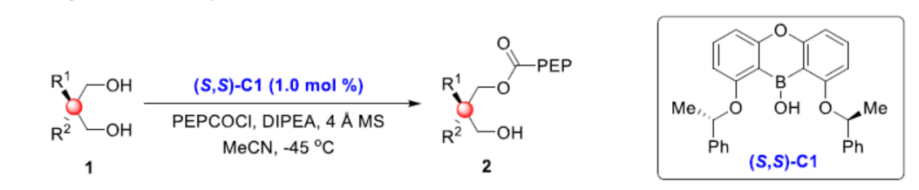
正文:
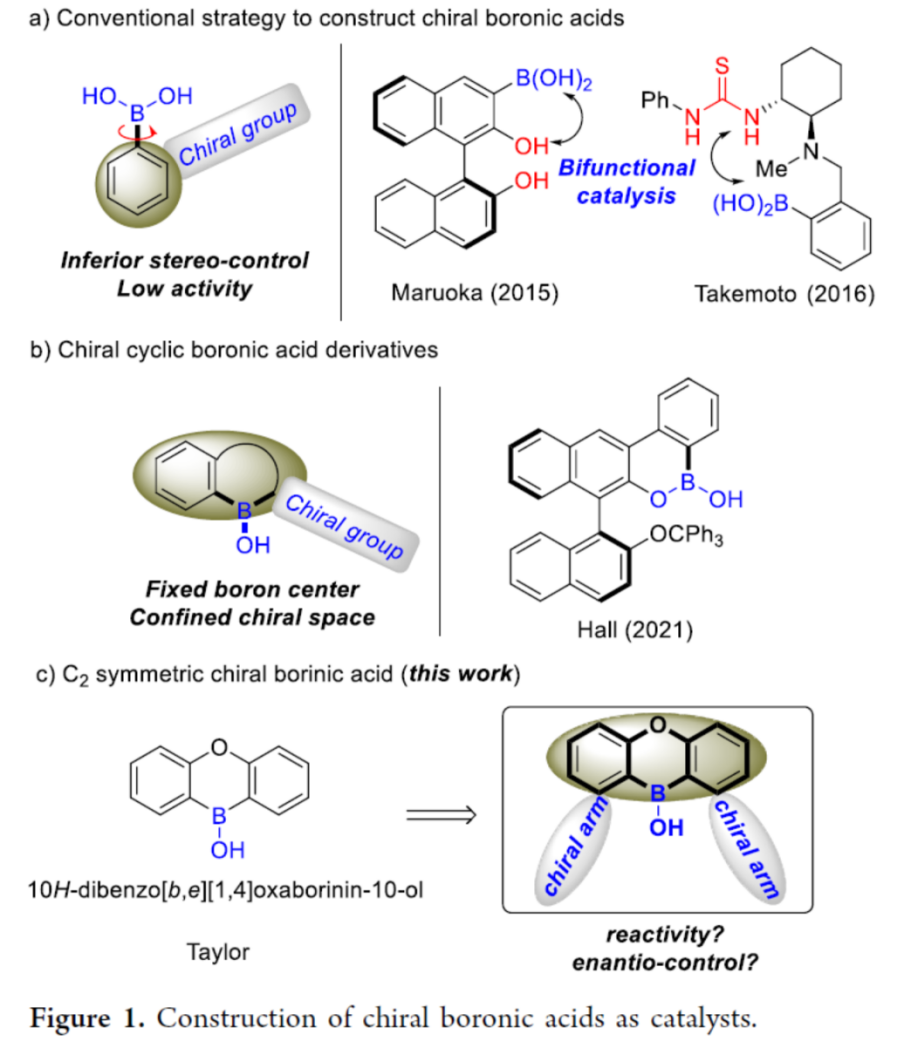
近年来,通过硼酸催化剂促进的合成转化方法学的相关研究,已经逐渐受到有机合成化学家的广泛关注[1]。然而,对于通过手性硼酸催化剂参与对映选择性合成转化方法学的研究,目前却较少有相关的文献报道 (Figure 1)[2]-[4]。这里,受到前期对于二芳基硼酸以及oxaboraanthracene催化活性与稳定性相关研究报道 (Figure 1c)[5]的启发,南京大学的郑文华课题组成功设计出一种全新的通过具有C2-对称性的手性硼酸催化剂促进的采用2,2-二取代-1,3-丙二醇参与的催化去对称化反应方法学。
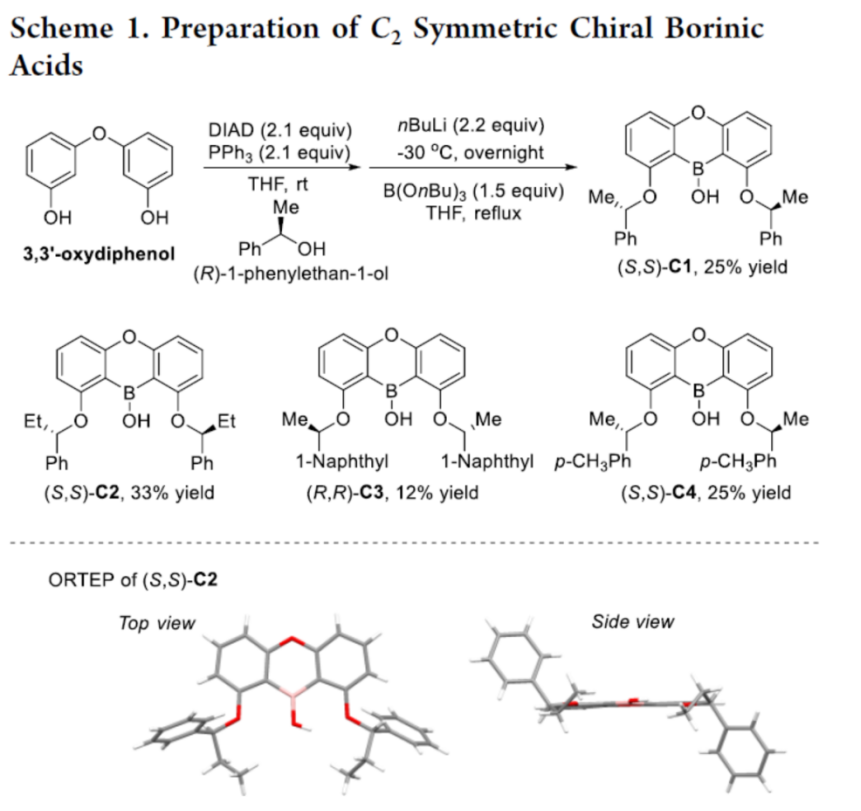
首先,作者成功合成出四种全新的具有C2-对称性的手性硼酸催化剂 (Scheme 1)。
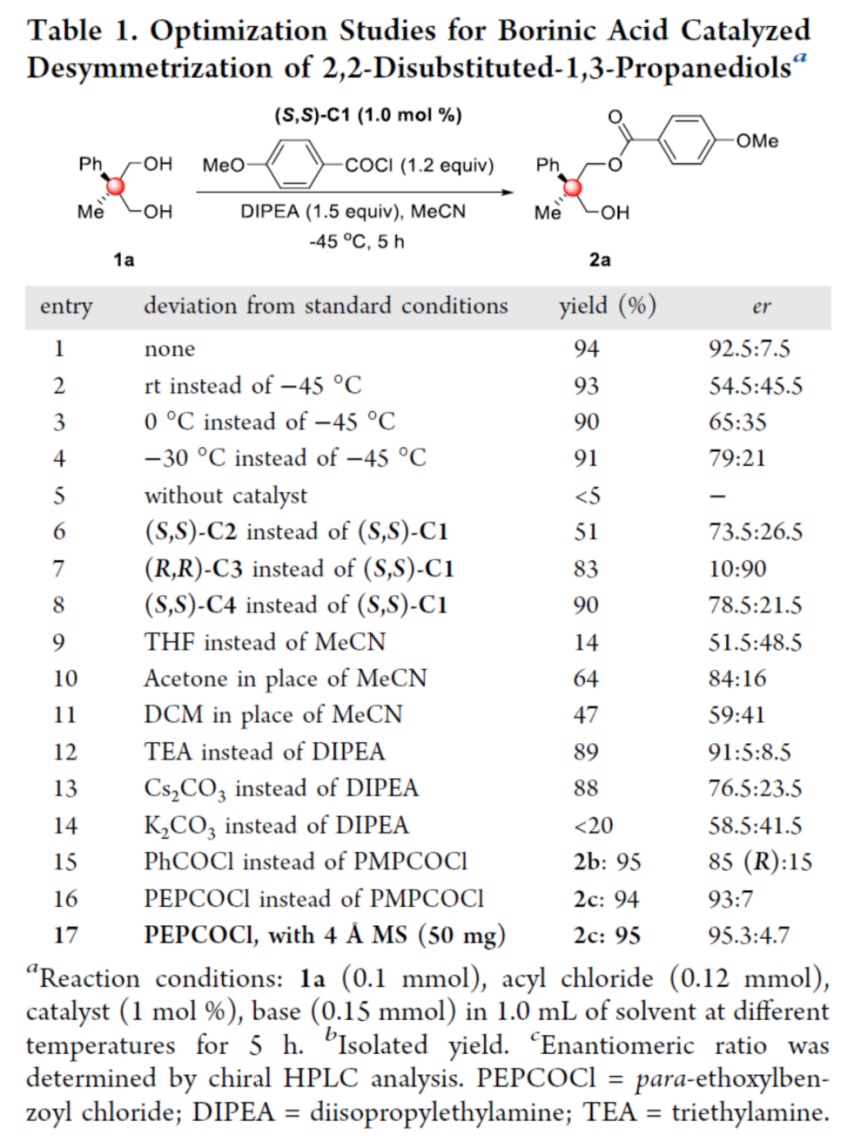
之后,作者采用2-苯基-2-甲基-1,3-丙二醇1a与4-甲氧基苯甲酰氯作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用(S, S)-C1作为催化剂,DIPEA作为碱,4 Å MS作为添加剂,MeCN作为反应溶剂,反应温度为-45 oC,最终获得95%收率的手性产物2a (95.3:4.7 er)。
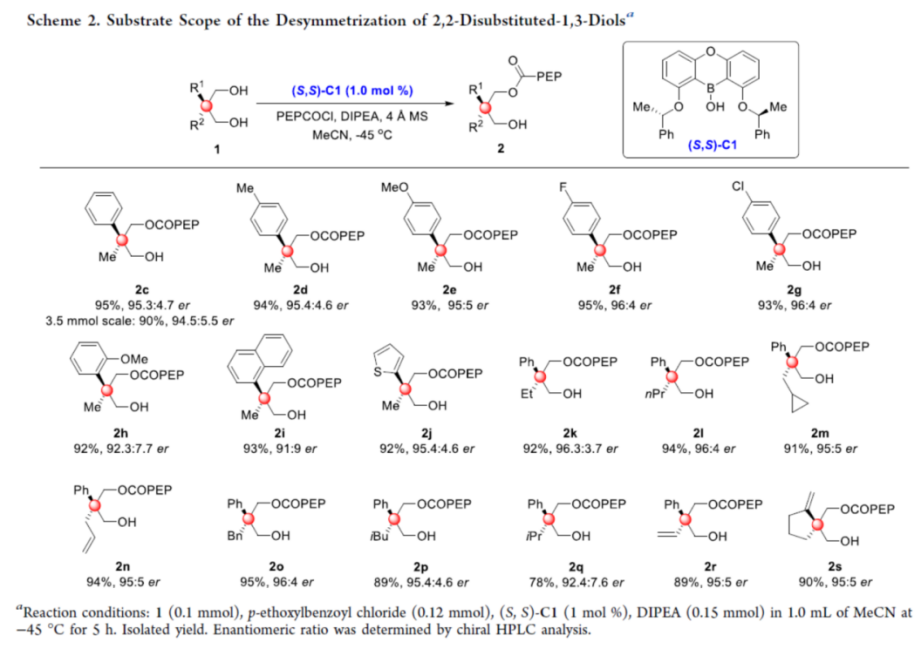
在上述的最佳反应条件下,作者对一系列2,2-二取代-1,3-丙二醇底物(Scheme 2)的应用范围进行深入研究。

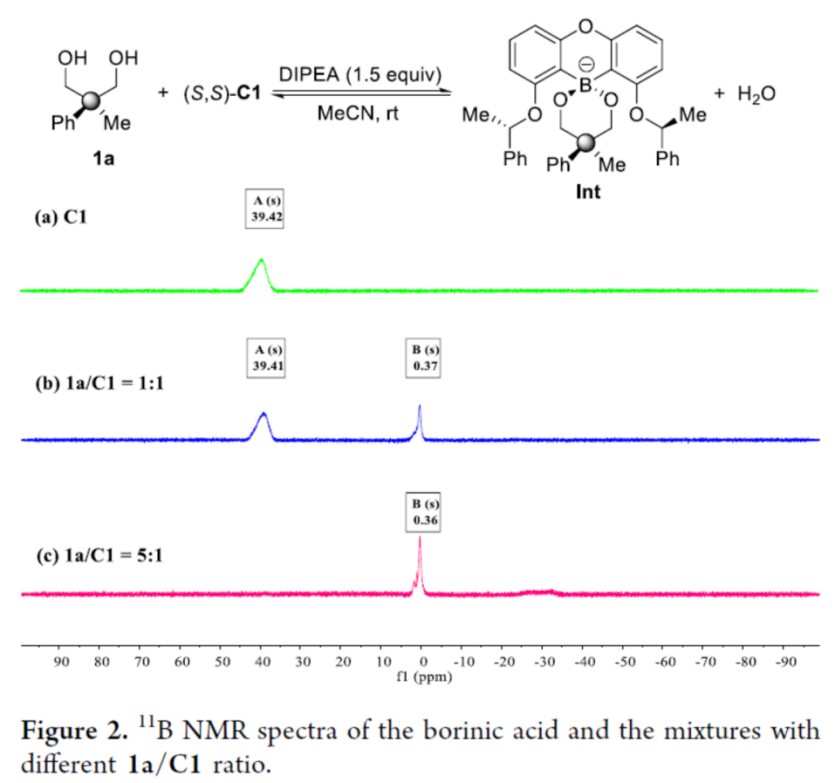
同时,作者通过一系列11B NMR实验,对硼酸催化剂与底物之间的相互作用进行深入研究 (Figure 2)。

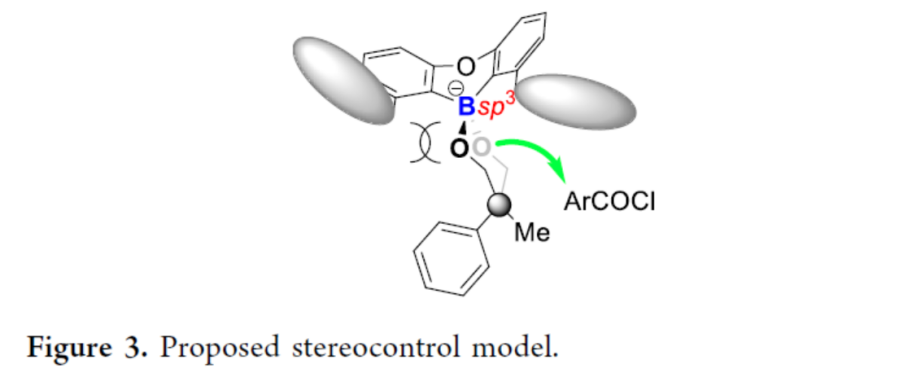
基于上述的实验研究,作者提出一种合理的立体选择性控制模型 (Figure 3)。
总结:
南京大学的郑文华课题组成功设计出一种全新的通过具有C2-对称性的手性硼酸催化剂促进的采用2,2-二取代-1,3-丙二醇参与的催化去对称化反应方法学,进而成功完成一系列具有四级碳立体中心的手性二醇分子的构建。这一全新的去对称化策略具有广泛的底物范围、优良的官能团兼容性以及优良的对映选择性等优势。
参考文献:
- [1] (a) E. Dimitrijević, M. S. Taylor, ACS Catal. 2013, 3, 945. doi: 10.1021/cs4000848. (b) I. Georgiou, G. Ilyashenko, A. Whiting, Acc. Chem. Res. 2009, 42, 756. doi: 10.1021/ar800262v. (c) D. G. Hall, Chem. Soc. Rev. 2019, 48, 3475. doi: 10.1039/C9CS00191C. (d) B. J. Graham, R. T. Raines, J. Org. Chem. 2022, doi: 10.1021/acs.joc.2c01695.
- [2] T. Hashimoto, A. O. Galvez, K. Maruoka, J. Am. Chem. Soc. 2015, 137, 16016. doi: 10.1021/jacs.5b11518.
- [3] N. Hayama, R. Kuramoto, T. Földes, K. Nishibayashi, Y. Kobayashi, I. Pápai, Y. Takemoto, J. Am. Chem. Soc. 2018, 140, 12216. doi: 10.1021/jacs.8b07511.
- [4] A. Adamczyk-Wozniak, K. M. Borys, A. Sporzynski, Chem. Rev. 2015, 115, 5224. doi: 10.1021/cr500642d.
- [5] (a) M. S. Taylor, Acc. Chem. Res. 2015, 48, 295. doi: 10.1021/ar500371z. (b) E. Dimitrijević, M. S. Taylor, Chem. Sci. 2013, 4, 3298. doi: 10.1039/C3SC51172C. (c) K. A. D’Angelo, M. S. Taylor, J. Am. Chem. Soc. 2016, 138, 11058. doi: 10.1021/jacs.6b06943. (d)V. Dimakos, H. Y. Su, G. E. Garrett, M. S. S. Taylor, J. Am. Chem. Soc. 2019, 141, 5149. doi:10.1021/jacs.9b01531.
- [6] (a) A. Adamczyk-Wozniak, K. M. Borys, A. Sporzynski, Chem. Rev. 2015, 115, 5224. doi: 10.1021/cr500642d. (b) L. M. Greig, B. M. Kariuki, S. Habershon, N. Spencer, R. L. Johnston, K. D. M. Harris, D. Philp, New J. Chem. 2002, 26, 701. doi: 10.1039/B110285K.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载

















No comments yet.