本文作者:杉杉
导读
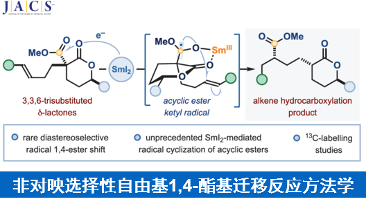
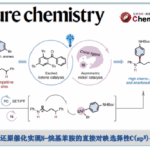
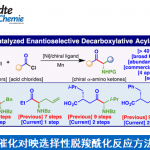
近日,Manchester大学的D. J. Procter课题组在J. Am. Chem. Soc.中发表论文,报道一种全新的通过SmI2促进的3,3,6-三取代δ-内酯的非对映选择性自由基1,4-酯基迁移反应方法学,进而成功完成一系列烯基氢羧基化分子的构建。
Diastereoselective Radical 1,4-Ester Migration: Radical Cyclizations of Acyclic Esters with SmI2
C. Morrill, Á. Peter, I. Amalina, E. Pye, G. E. M. Crisenza, N. Kaltsoyannis, D. J. Procter, J. Am. Chem. Soc. 2022, ASAP. doi: 10.1021/jacs.2c05972.
正文
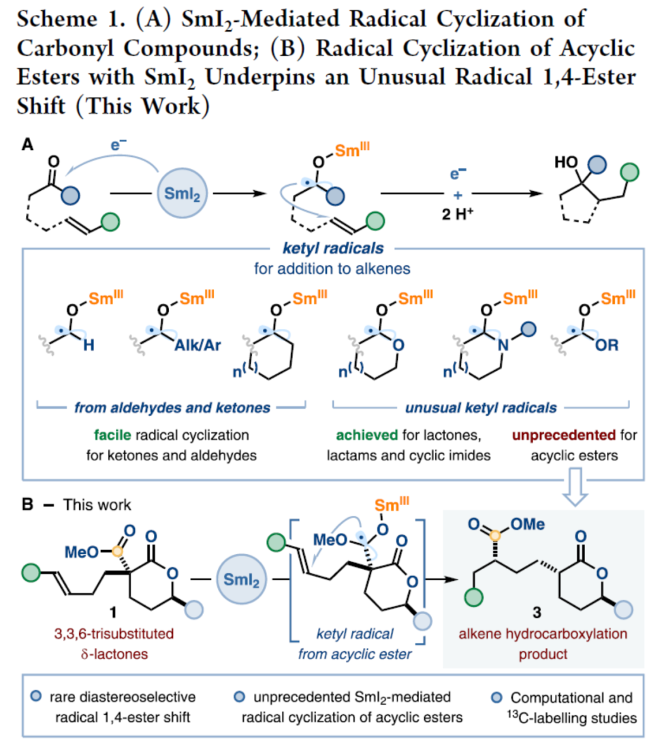
自由基环化是区域与立体选择性地构建复杂有机分子的有效策略之一[1]。在过去的几十年里,已经成功设计出多种通过SmI2促进的羰基化合物的自由基环化反应方法学[2]-[10] (Scheme 1A)。然而,采用SmI2促进的通过非环酯类分子参与的自由基环化反应方法学,目前却较少有相关的研究报道[11]-[12]。
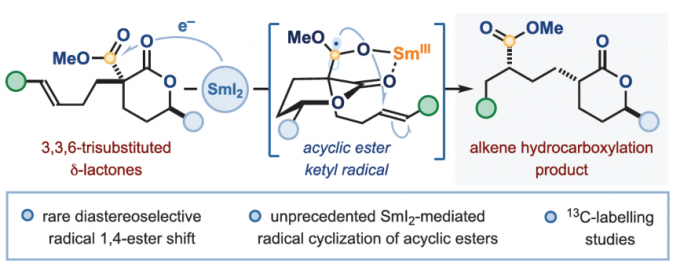
这里,受到本课题组前期对于采用SmI2·H2O·Et3N成功将一系列非环酯类分子还原为相应的羰基自由基负离子等价物[12]相关研究报道的启发,Manchester大学的D. J. Procter课题组成功设计出一种全新的通过SmI2促进的3,3,6-三取代δ-内酯的非对映选择性自由基1,4-酯基迁移反应方法学 (Scheme 1B)。
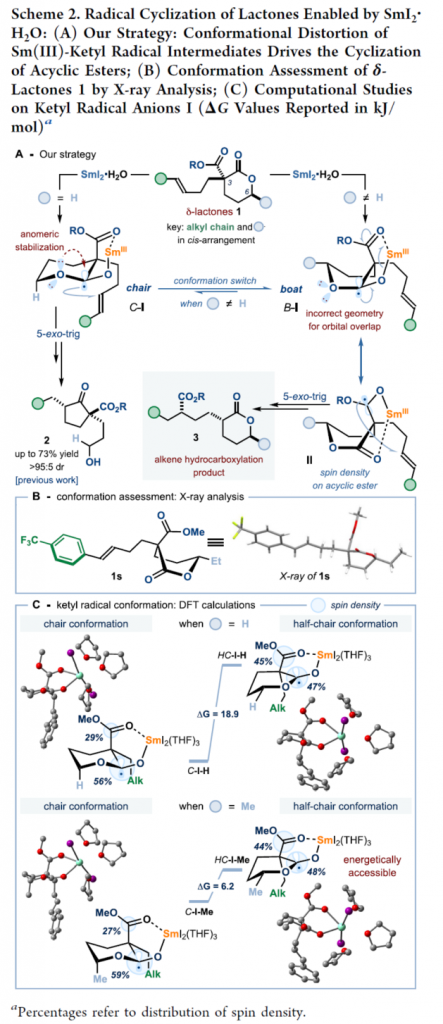
首先,Procter团队通过X-射线晶体学分析以及DFT计算,对反应过程中δ-内酯与SmI2作用之后的反应活性构象及其后续的环化路径进行深入研究 (Scheme 2)。
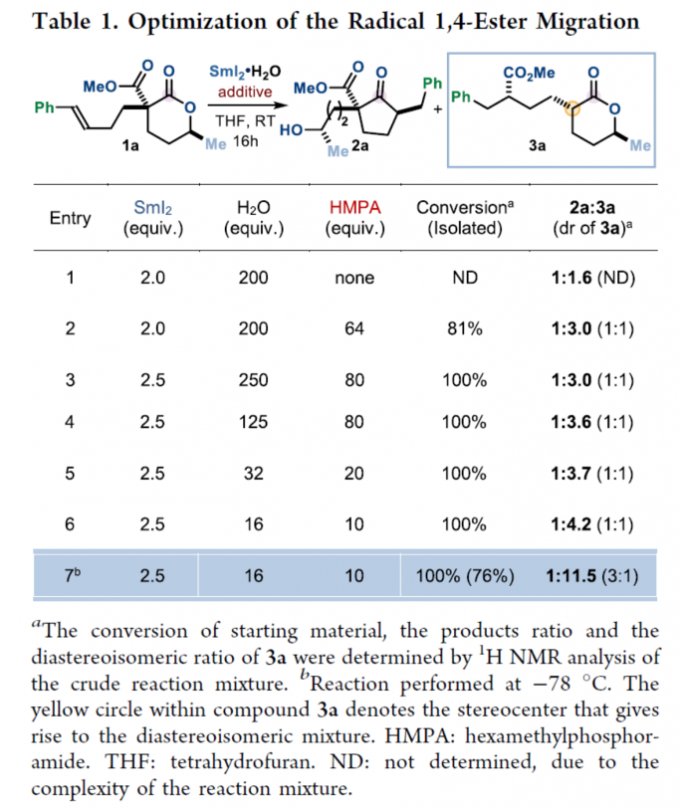
之后,作者采用6-甲基取代的δ-内酯衍生物1a作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用SmI2·H2O作为还原剂,HMPA作为添加剂,THF作为反应溶剂,反应温度为-78oC,最终获得76%收率的1,4-酯基迁移产物3a (dr = 3:1)。
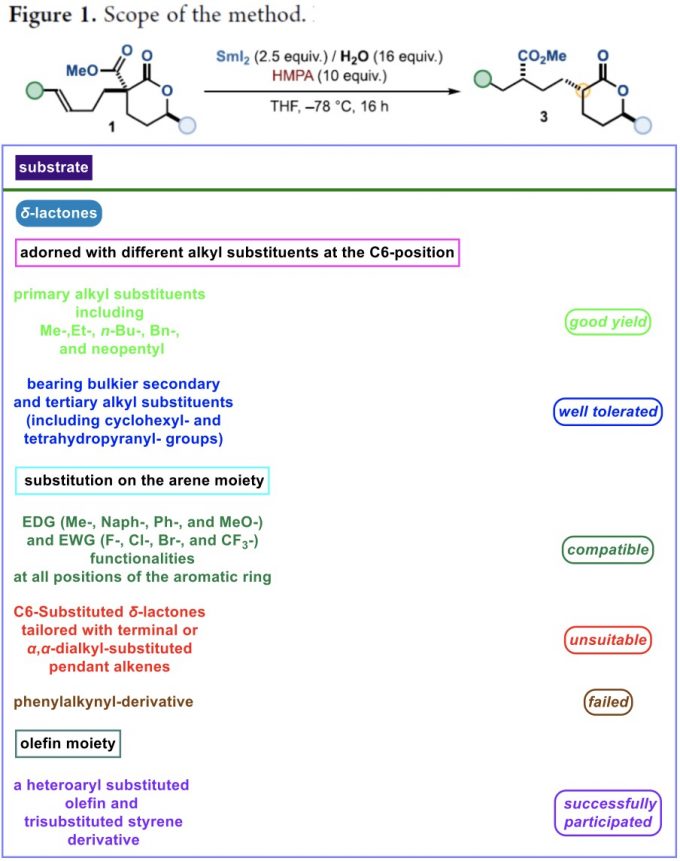
在上述的最佳反应条件下,作者对一系列δ-内酯底物 (Figure 1)的应用范围进行深入研究。
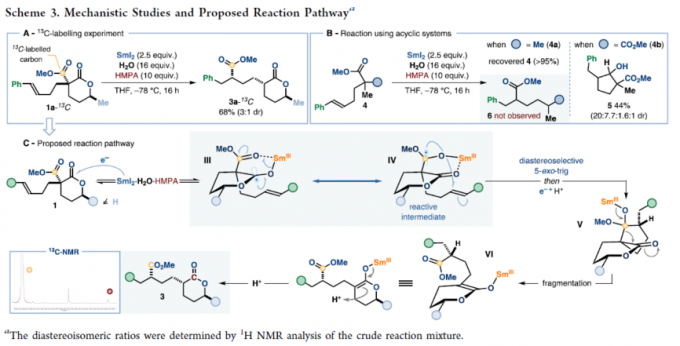
接下来,作者通过13C-同位素标记实验的相关研究表明,由内酯分子中非环酯取代基团形成的Sm(III)-羰基自由基负离子在自由基环化过程中能够与分子中的烯基单元结合 (Scheme 3A)。之后,该小组通过对1中内酯环结构单元反应活性的进一步研究观察到,非环酯基团的SET还原并非仅限于具有内酯结构单元的底物。然而,内酯结构单元对于促进螺环中间体 (在自由基环化过程之后形成)经历后续的碎片化过程,最终形成酯基迁移产物尤为关键 (Scheme 3B)。通过1,4-酯基迁移,能够形成更加稳定的环状Sm(III)-enolate中间体。基于上述的实验研究,作者提出如下合理的反应机理 (Scheme 3C)。
总结
Manchester大学的D. J. Procter课题组报道一种全新的通过SmI2促进的3,3,6-三取代δ-内酯的非对映选择性自由基1,4-酯基迁移反应方法学,进而成功完成一系列烯基氢羧基化分子的构建。这一全新的自由基1,4-酯基迁移策略具有优良的非对映选择性以及优良的官能团兼容性等优势。
参考文献
- [1] H. Huang, M. H. Garduño-Castro, C. Morrill, D. J. Procter, Chem. Soc. Rev. 2019, 48, 4626. doi: 10.1039/C8CS00947C.
- [2] M. Yan, J. C. Lo, J. T. Edwards, P. S. Baran, J. Am. Chem. Soc. 2016, 138, 12692. doi: 10.1021/jacs.6b08856.
- [3] G. A. Molander, C. R. Harris, Chem. Rev. 1996, 96, 307. doi: 10.1021/cr950019y.
- [4] Á. Péter, D. J. Procter, Chimia 2019, 74, 18. doi: 10.2533/chimia.2020.18.
- [5] Á. Péter, S. Agasti, O. Knowles, E. Pye, D. J. Procter, Chem. Soc. Rev. 2021, 50, 5349. doi: 10.1039/D0CS00358A.
- [6] S. Agasti, N. A. Beattie, J. J. W. McDouall, D. J. Procter, J. Am. Chem. Soc. 2021, 143, 3655. doi: 10.1021/jacs.1c01356.
- [7] Á. Péter, G. E. M. Crisenza, D. J. Procter, J. Am. Chem. Soc. 2022, 144, 7457. doi: 10.1021/jacs.2c02188.
- [8] H. Huang, J. J. W. McDouall, D. J. Procter, Angew. Chem., Int. Ed. 2018, 57, 4995. doi: 10.1002/anie.201800667.
- [9] S. Shi, M. Szostak, Org. Lett. 2015, 17, 5144. doi: 10.1021/acs.orglett.5b02732.
- [10] E. Prasad, R. A. Flowers, J. Am. Chem. Soc. 2005, 127, 18093. doi: 10.1021/ja056352t.
- [11] M. Szostak, M. Spain, K. A. Choquette, R. A. Flowers, D. J. Procter, J. Am. Chem. Soc. 2013, 135, 15702. doi: 10.1021/ja4078864.
- [12] M. Szostak, M.Spain, D. J. Procter, Chem. Commun. 2011, 47, 10254. doi: 10.1039/C1CC14014K.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载





















No comments yet.