本文作者:杉杉
导读
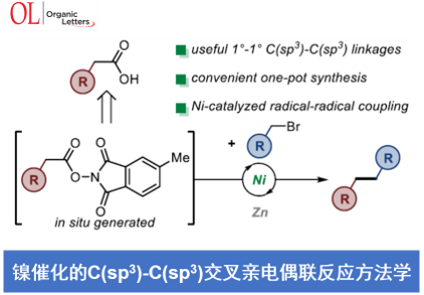
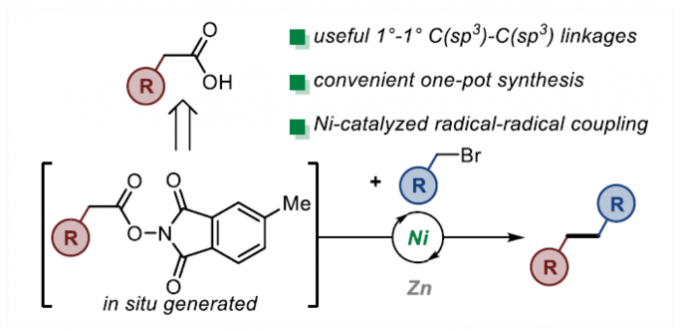
近日,Wisconsin大学的D. J. Weix课题组在Org. Lett.中发表论文,报道一种全新的采用镍催化剂促进的非活化烷基溴与原位形成的NHP酯 (N-hydroxyphthalimide esters)之间的交叉亲电偶联 (cross-electrophile coupling)反应方法学,进而成功完成一系列具有1°/1° C(sp3)-C(sp3)键的有机分子的构建。
Nickel-Catalyzed C(sp3)-C(sp3) Cross-Electrophile Coupling of In Situ Generated NHP Esters with Unactivated Alkyl Bromides
Kang, D. J. Weix, Org. Lett. 2022, ASAP. doi: 10.1021/acs.orglett.2c00805.
正文:
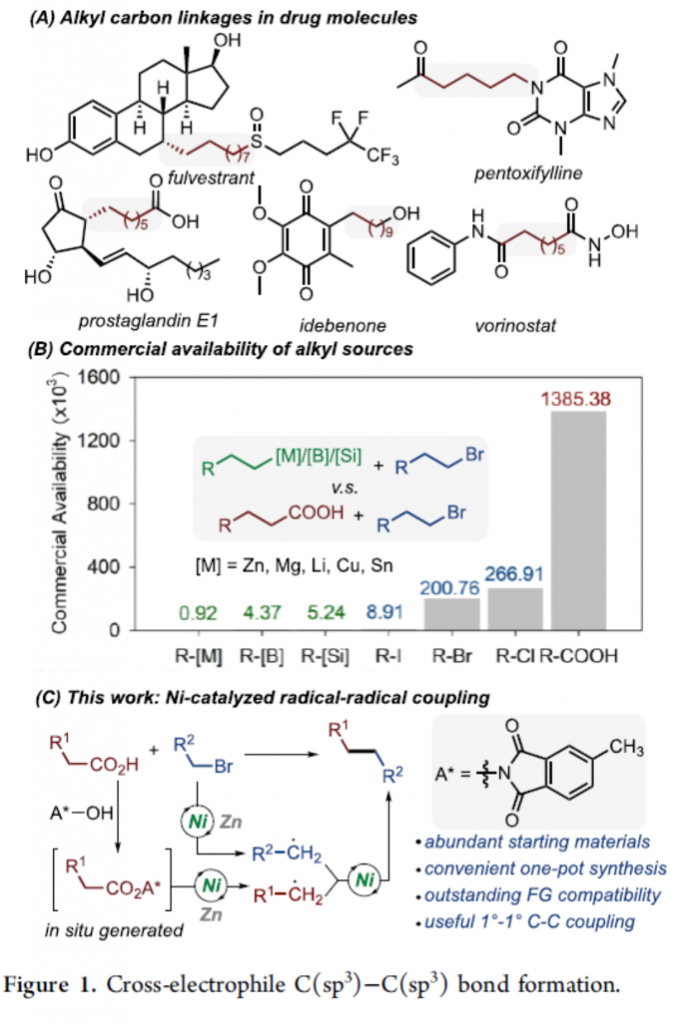
具有C(sp3)-C(sp3)键的有机结构单元广泛存在于各类天然产物以及药物分子中(Figure 1A)。目前,一系列烷基亲核底物与烷基亲电底物之间的C(sp3)-C(sp3)交叉偶联反应方法学的相关研究,已经备受有机合成化学家的广泛关注[1] (Figure 1B)。然而,对于C(sp3)-C(sp3)交叉亲电偶联反应方法学的相关研究,仍面临诸多挑战[2]-[3]。这里,受到近年来对于自由基C(sp3)-C(sp3)键交叉亲电偶联反应方法学[4]-[7]、通过非活化烷基羧酸与非活化烷基溴之间的脱羧交叉偶联反应方法学[8]以及多金属光氧化还原 (multimetallic photoredox)反应方法学[9]相关研究报道的启发,Wisconsin大学的D. J. Weix课题组成功设计出一种全新的采用镍催化剂促进的非活化烷基溴与原位形成的NHP酯 (N-hydroxyphthalimide esters)之间的交叉亲电偶联反应 (cross-electrophile coupling)方法学 (Figure 1C)。
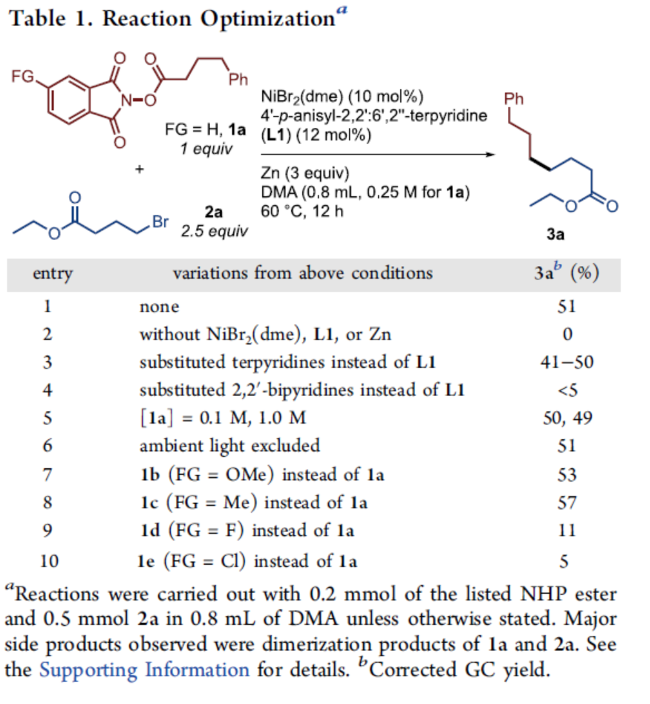
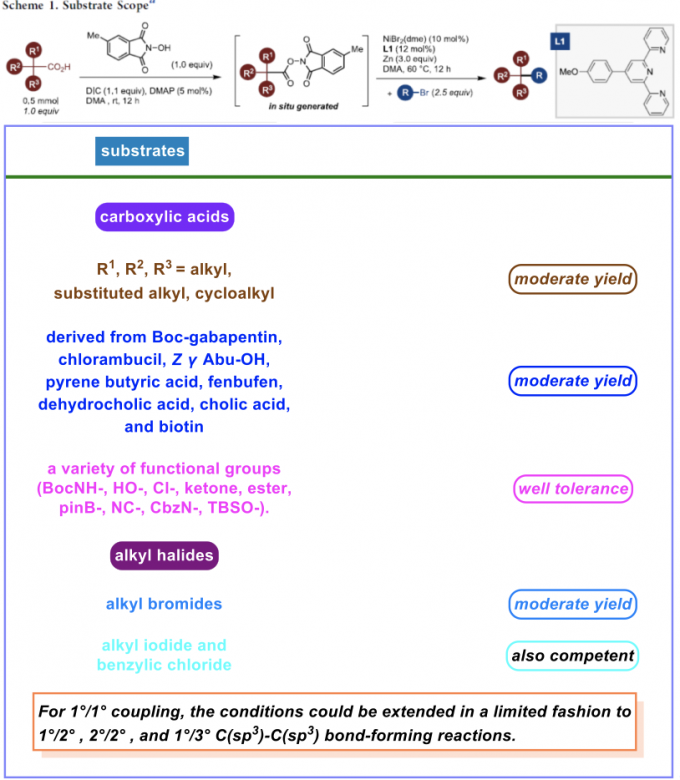
首先,作者采用NHP酯衍生物1c与烷基溴2a作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用NiBr2(dme)作为催化剂,L1作为配体,Zn粉作为还原剂,DMA作为反应溶剂,反应温度为60oC,最终获得57%收率的偶联产物3a。
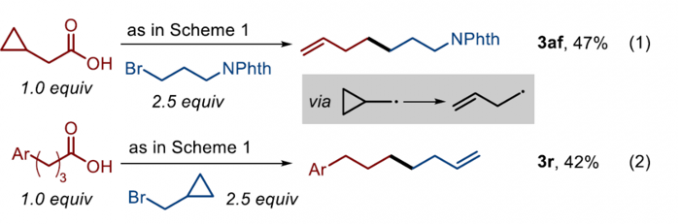
在上述的最佳反应条件下,作者对一系列相关底物 (Scheme 1)的应用范围进行深入研究。
之后,该小组通过对反应机理的初步研究表明,偶联过程中涉及烷基自由基中间体的形成。
总结
Wisconsin大学的D. J. Weix课题组报道一种全新的镍催化非活化烷基溴与原位生成NHP酯之间的交叉亲电偶联反应方法学,进而成功完成一系列具有1°/1° C(sp3)-C(sp3)键的有机分子的构建。这一全新的合成转化策略具有广泛的底物应用范围、良好的反应收率以及优良的官能团兼容性等优势。
参考文献
- [1] (a) X. Hu, Chem. Sci. 2011, 2, 1867. doi: 10.1039/C1SC00368B.
- (b) G. Fu, ACS Cent. Sci. 2017, 3, 692. doi: 10.1021/acscentsci.7b00212.
- [2] C. E. I. Knappke, S. Grupe, D. Gartner, M. Corpet, C. Gosmini, A. Jacobi von Wangelin, Chem. Eur. J. 2014, 20, 6828. doi: 10.1002/chem.201402302.
- [3] J. Gu, X. Wang, W. Xue, H. Gong, Org. Chem. Front. 2015, 2, 1411. doi: 10.1039/C5QO00224A.
- [4] (a) D. J. Weix, Acc. Chem. Res. 2015, 48, 17675. doi: 10.1021/acs.accounts.5b00057.
- (b) S. Biswas, D. J. Weix, J. Am. Chem. Soc. 2013, 135, 16192. doi: 10.1021/ja407589e.
- [5] R. T. Smith, X. Zhang, J. A. Rincon, J. Agejas, C. Mateos, M. Barberis, S. Garcia-Cerrada, O. de Frutos, D. W. C. MacMillan, J. Am. Chem. Soc. 2018, 140, 17433. doi: 10.1021/jacs.8b12025.
- [6] A. B. Sanford, T. A. Thane, T. M. McGinnis, P. Chen, X. Hong, E. R. Jarvo, J. Am. Chem. Soc. 2020, 142, 5017. doi: 10.1021/jacs.0c01330.
- [7] T. Yang, Y. Wei, M. J. Koh, ACS Catal. 2021, 11, 6519. doi: 10.1021/acscatal.1c01416.
- [8] S. J. McCarver, J. X. Qiao, J. Carpenter, R. M. Borzilleri, M. A. Poss, M. D. Eastgate, M. M. Miller, D. W. C. MacMillan, Angew. Chem., Int. Ed. 2017, 56, 728. doi: 10.1002/anie.201608207.
- [9] (a) W. Liu, M. N. Lavagnino, C. A. Gould, J. Alcázar, D. W. C. MacMillan, Science 2021, 374, 1258. doi: 10.1126/science.abl4322.
- (b) C. P. Johnston, R. T. Smith, S. Allmendinger, D. W. C. MacMillan, Nature 2016, 536, 322. doi: 10.1038/nature19056.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载




















No comments yet.