投稿作者 alberto-caeiro
背景介绍及结构测定
贝壳类海洋生物的生物毒性可分为5种:麻痹性贝类中毒(paralyticshellfishpoison-ing/PSP)、腹泻性贝类中毒(diarrheticshellfishpoisoning/DSP)、记忆缺失性贝类中毒(amnesic shellfish poisoning/ASP)、神经性贝类中毒(neurotoxicshellfishpoisoning/NSP)和最后的azaspiracidshellfish poisoning/AZP,而AZP是2004年由联合国粮农组织单独确定的第五类贝类中毒,即本次全合成工作的主角分子。
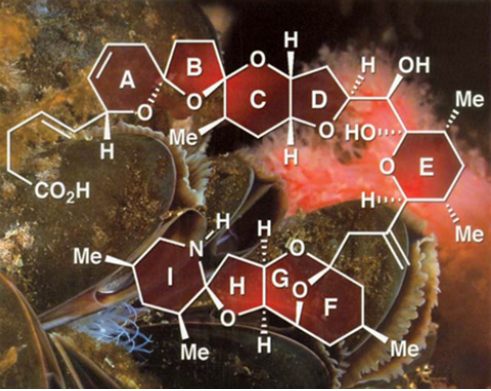
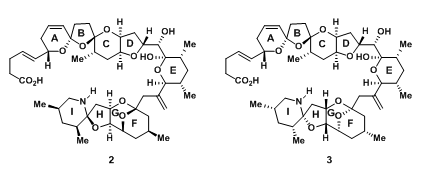
故事的开始是1995年的一起食品中毒事件。1995年的新西兰有一起DSP案例,患者有与DSP相同的症状,恶心、呕吐和严重的腹泻,然而在后面的调查中发现,这是一起全新的案例。患者的中毒源可以追溯到食用了一种养殖于爱尔兰西海岸Killary港口的一种贻贝(Mytilus edulis),随后,在对港口的水进行检测中,并没有发现含有任何已知的毒素或者可产生有毒物质的浮游生物。但是,在将此类贝壳提取物进行小鼠注射实验时,小鼠有严重的PSP症状,并于20分钟内死亡。事情的下一步进展是在1997年,爱尔兰的西北海岸也有几起相同的中毒事件被报道。不明中毒源和巨大的毒性危害人们的安全,于是许多课题组都开展了针对于此的研究。在1998年,Yasumoto和Satake报道了从M. edulis贝类中分离出的制毒物质azaspiracid-1,并且给出了四种(2,3及它们的对映体)可能的结构[1],如图一。
图1:Originally Proposed Structure for azaspiracid-1
为了研究azaspiracid-1的化学和生物学性质,需要有足够的充足的天然产物。显然,故事发展到这里,合成化学家就要开始登场了。可是,故事并不是那么的简单。在全合成之前,更加重要的一件事需要解决,那就是azaspiracid-1的准确结构到底是怎样的,这对全合成也是至关重要的。而实际上,在达成目标之前,全合成对化合物的结构解析,起着至关重要的作用(play a central role in the azaspiracid-1 saga—— cite from this book)。
从原始猜测的结构可以看出其复杂程度——9个环及20个手性中心。在其结构中,有两个四环结构,二螺缩酮并四氢呋喃环系ABCD和N杂螺环并桥环环系FGHI,以及中间含有环状半缩酮的E环。针对设想结构的ABC三环结构,几个课题组对其进行了合成工作都表明,设想结构是一个反热力学的结构。由下图2可以看出,结构4中O的孤对电子与邻位的C-O键的反键轨道有重叠,形成anomeric stabilization使结构有更好的稳定性,而在C-13位的差向异构体5可以看出它有两个这样的重叠稳定作用,在热力学上应该更加稳定。在2001年,两个课题组分别通过实验证明了这种猜想[2, 3]。但是,在各种热力学或者动力学控制的反应条件下,都只得到了C-13位的差向异构体5。于是,如何得到设想结构的ABCD4环结构是当时全合成的一个大难题!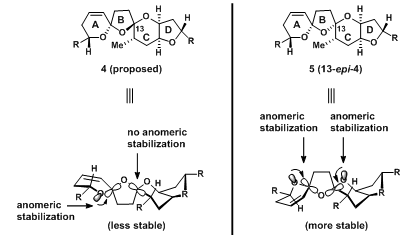
图2:ProposedStructure4&5 C13-epi-4
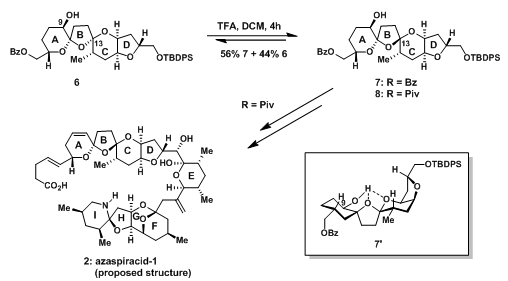
2001年,K. C. Nicolaou教授成功的合成了设想结构的ABCD4环结构[4]。如下图3所示,通过在C-9位加入一个羟基作为手性控制基团,以抵消设想结构中热力学上的不利效果。在TFA催化的一个平衡反应中,中间体7‘由于C-9羟基与氧的氢键作用,使平衡有右移的动力,最终经平衡反应得到56%的7,44%的6。再得到充足的ABCD4环结构碎片后,K. C. Nicolaou教授于2003年完成了设想结构2,3的全合成工作[5]。然而,完成了设想结构之后并不能宣告工作的完结,有关azaspiracid-1的谜题却是越来越扑朔迷离。实际的天然产物只是一个物质,而合成的2,3确实E环的异构体。另外,在详细对比天然产物与合成产物的NMR谱图之后发现,他们并不是真正的天然产物azaspiracid-1!那么问题到底出在哪里了呢?
图3:TFA-Mediated Equilibration & Synthesis of the Proposed Azaspiracid-1
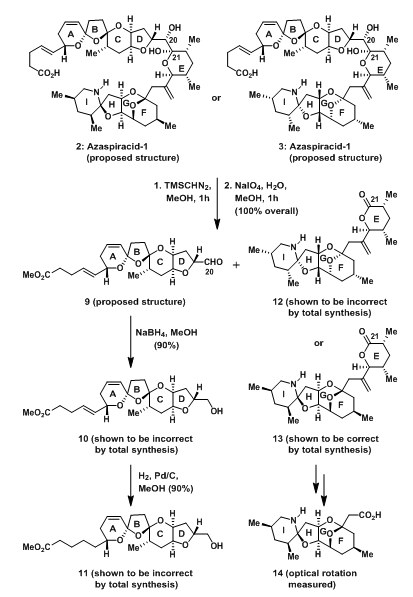
为了解决这个结构确认难题,K. C. Nicolaou教授与发现此物质的Satake课题组展开了合作,希望通过化学合成和天然产物降解分析相结合,得到准确的结构式。Satake课题组对天然产物进行了小量的降解反应,以得到降解物的NMM-H谱图,过程如图4所示。需要说明的是,所有结构都是以最初设想结构式表示!
图5:Degradative Studies on Azaspiracid-1
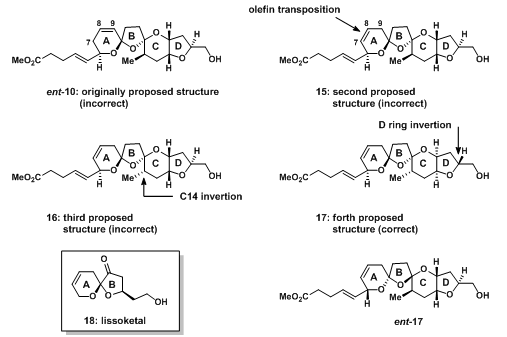
化学合成在以前的路线上稍加修饰,得到的谱图与降解碎片比较,以确定其准确的结构。K. C. Nicolaou教授合成了FGHI四环结构12和13,通过与降解产物比较,确定其结构为13。但由天然产物降解得到的12和13不能进行旋光度测试,于是将进一步反应的14的旋光度与合成的片段相比较,最终确定FGHI4环结构以及碎片13的绝对构型为14所示,但在ABCD4环的结构确定上却没有太大的进展,天然产物降解得到的片段与合成的片段在NMR-H谱上有明显的不同,但是,却给我们提供了一条其他的线索。在1997年发现的另一种海洋内的天然产物lissoketal[6](图6)中,同样有类似的缩酮结构,但它的双键与缩酮并不共轭,而它的NMR-H谱却与azaspiracid-1的谱图在微观结构中,特征峰有很大的相似性。于是我们猜想,是否azaspiracid-1的双键位移至了C7-C8为呢?双键移位后的碎片在NMR-H谱上确实与天然产物降解更加匹配,可是它们的稳定性却有很大差别。15对酸诱导的异构化反应很敏感,而azaspiracid-1及降解碎片对此反应都有很好的耐受性。这说明azaspiracid-1是热力学稳定的,因此在产物中有两个端基稳定效应作用(stabilizinganomeric effect)。在这个4环体系中,共有7个手性中心64个异构体,考虑到两个端基稳定最用以及奥弗豪塞尔核效应(Nuclear Overhauser Effect[7])(维基百科),范围缩小到2个,即16与17,最终NMR-H谱图匹配得到最终结构为17。但由于azaspiracid-1的量不足,不能用于旋光度测定,并不能确定其绝对够型。
图6:Molecular Structure of Lissoketal 18 & Revised Compounds during the Structure Elucidation
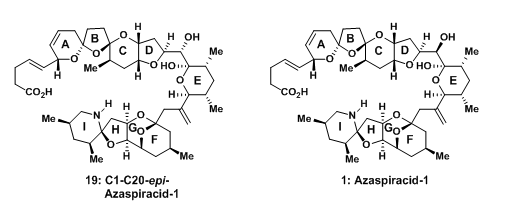
于是,在有这些结构信息的条件下,两种azaspiracid-1可能的结构19和1(图7)都被K. C. Nicolaou教授课题组完成合成,在2004年,azaspiracid-1的结构终于为人们所认知[8](14),并确定为结构式1!
图7:molecularstructureof 19 & 1
在2006年,K. C. Nicolaou教授以一条更短更高效的方法重新完成了azaspiracid-1的全合成,2007年,D. A. Evans教授也完成了ent-1的全合成。后面,主要介绍的是K. C. Nicolaou教授在2006年的合成工作以及D. A. Evans教授在2007年的合成工作[9]。
参考文献
- Satake, K. Ofuji, H. Naoki, K. J. James, A. Furey, T. McMahon, J. Silke, T. Yasumoto*, J. Am. Chem. Soc., 1998, 120, 9967;
- B. Dounay, C. J. Forsyth*, Org. Lett., 2001, 3, 975;
- G. Carter, D. E. Graves*, Tetrahedron Lett. 2001, 42, 6035;
- C. Nicolaou, W. Qian, F. Bernal, N. Uesaka, P. M. Pihko, J. Hinrichs, Angew. Chem. Int. Ed., 2001, 40, 4068;
- a) K. C. Nicolaou, Y. Li, N. Uesaka, T. V. Koftis, S. Vyskocil, T. Ling, M. Govindasamy, W. Qian, F. Bernal, D. Y-K. Chen, Angew. Chem. Int. Ed., 2003, 42, 3643; b) K. C. Nicolaou, Y. Li, N. Uesaka, T. V. Koftis, S. Vyskocil, T. Ling, M. Govindasamy, W. Qian, F. Bernal, D. Y-K. Chen, Angew. Chem. Int. Ed., 2003, 42, 3649;
- Hopmann, D. J. Faulkner, Tetrahedron Lett, 1997, 38, 169;
- Nuclear Overhauser Effect=https://en.wikipedia.org/wiki/Nuclear_Overhauser_effect;
- a) K. C. Nicolaou, S. Vyskocil, T. V. Koftis, Y. M. A. Yamada, T. Ling, D. Y-K. Chen, W. Tang, G. Petrovic, M. O. Frederick, Y. Li, Angew. Chem. Int. Ed., 2004, 43, 4312; b) K. C. Nicolaou, S. Vyskocil, T. V. Koftis, Y. M. A. Yamada, T. Ling, D. Y-K. Chen, W. Tang, G. Petrovic, M. O. Frederick, Y. Li, Angew. Chem. Int. Ed., 2004, 43, 4318; c) K. C. Nicolaou*, T. V. Koftis, S. Vyskocil, G. Petrovic, W-J Tang, M. O. Frederick, David Y.-K. Chen, Y-W Li, T-T. Ling, Y. M. A. Yamada,J. Am. Chem. Soc., 2006, 128, 2859;
- a) D. A. Evans, L. Kværnø, J. A. Mulder, B. Raymer, T. B. Dunn, A. Beauchemin, E. J. Olhava, M. Juhl, K. Kagechika, Angew. Chem. Int. Ed., 2007, 46, 4693; b) D. A. Evans, L. Kværnø, J. A. Mulder, B. Raymer, T. B. Dunn, A. Beauchemin, E. J. Olhava, M. Juhl, K. Kagechika, Angew. Chem. Int. Ed., 2007, 46, 4698; c) D. A. Evans, L. Kværnø, T. B. Dunn, A. Beauchemin, B. Raymer, J. A. Mulder, E. J. Olhava, M. Juhl, K. Kagechika, D. A. Favor, J. Am. Chem. Soc., 2008, 130, 16295;
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!























No comments yet.