本文作者:杉杉
导读
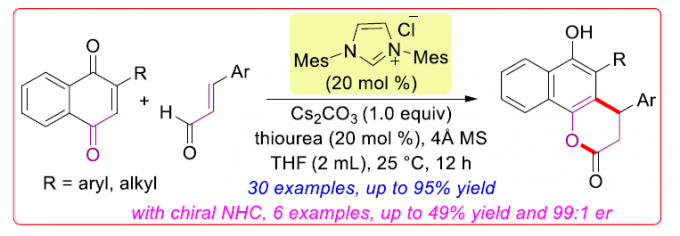
近日,印度科学研究所有机化学系Akkattu T. Biju课题组在Org. Lett.上发表论文,报道一种NHC催化α,β-不饱和醛与2-取代1,4-萘醌的[3+3]环化反应,合成一系列官能团化的二氢香豆素衍生物。机理研究表明,初始形成的NHC-高烯醇负离子(homoenolates)可进行Michael-异构化-内酯化串联过程,而非涉及α,β-不饱和酰基唑鎓(acylazolium)中间体的形成。此外,使用手性NHCs,可获得收率高达49%和er值高达99:1的产物。
Synthesis of Functionalized Dihydrocoumarins by NHC-Catalyzed [3+3] Annulation of Enals with 2‑Substituted Naphthoquinones
Sayan Shee, Soumen Barik, Arghya Ghosh, and Akkattu T. Biju* Org. Lett.2021, 23, 8039.
正文
官能团化的二氢香豆素是具有价值的杂环支架,广泛存在于天然产物和生物分子中。其中,多种3,4-二氢香豆素衍生物与生物活性有关,例如抗炎、抗癌、抗氧化和抗衰老特性。此外,其中一些化合物在香精和香料工业中得到了应用,并且在有机合成中也作为具有价值的中间体。鉴于这种杂环骨架的重要性,仍需开发一种更为温和合成官能团化二氢香豆素的方法。
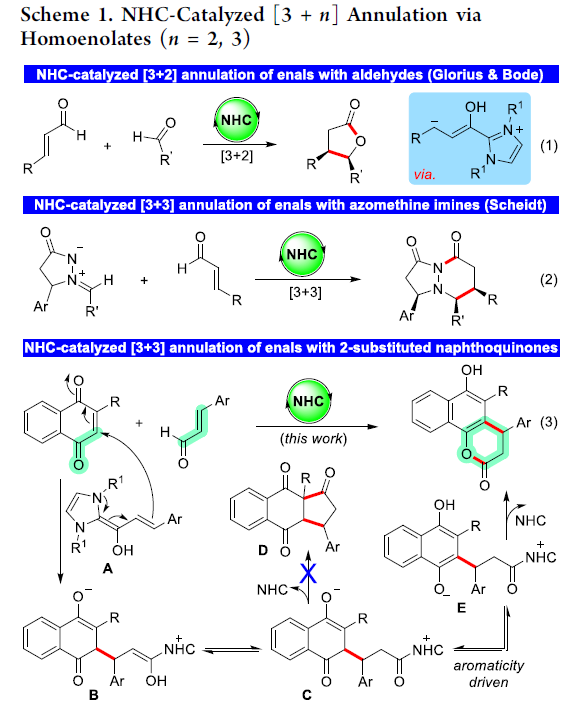
使用NHCs的有机催化对于醛的极性反转(umpolung)非常有用[1],并且亲核 Breslow中间体(酰基阴离子等价物)的形成是反应成功的关键[2]。Benzoin反应和 Stetter反应是两个经典的反应,涉及醛极性反转的过程。2004年,Glorius[3]和 Bode课题组[4]报道了将NHCs的极性反转概念扩展到α,β-不饱和醛。其中,生成的高烯醇负离子中间体(共轭极性反转)在[3+2]环化反应中被醛拦截,从而合成γ-丁内酯(Scheme 1, eq 1)。随后,也陆续实现了各种[3+2][5]、[3+3][6]、[3+4][7]和[3+8][8]环化反应。2007年,Scheidt课题组[9]报道了NHC催化α,β-不饱和醛与甲亚胺亚胺(azomethine imines)的[3+3]环化反应,实现双环杂环化合物的非对映选择性合成。
鉴于NHC-高烯醇负离子在[3+n]环化反应中的广泛应用,并考虑到高烯醇负离子与缺电子烯烃的环戊环化反应,作者设想,在[3+2]环化反应中可使用2-取代1,4-萘醌中缺电子双键拦截高烯醇负离子。令人惊讶的是,这些反应形成官能团化的二氢香豆素,而不是预期的三环环戊酮(eq 3)。从机理上讲,最初生成的高烯醇负离子A与2-取代萘醌进行Michael加成,形成烯醇化物中间体B,经互变异构化后形成酰基唑鎓(acylazolium)C。预期将分子内烯醇加成到NHC-唑鎓以形成环戊酮D,但中间体C经历了芳香性驱动的异构化以形成烯醇中间体E。最后,中间体E经分子内环化形成二氢香豆素,并再生NHC。在此,Akkattu T. Biju课题组报道一种NHC催化α,β-不饱和醛与2-取代1,4-萘醌的[3+3]环化反应,合成一系列官能团化的二氢香豆素衍生物,涉及Michael-异构化-内酯化串联过程。
首先,作者采用2-苯基萘醌1a与烯醛2a作为模型底物,进行了相关环化反应条件的优化筛选(Table 1)。确定最佳的反应条件为:采用4作为催化剂,Cs2CO3作为碱,硫脲和4Å MS作为添加剂,在THF溶剂中,25 oC下进行反应,最终获得84%收率的环化产物3a。
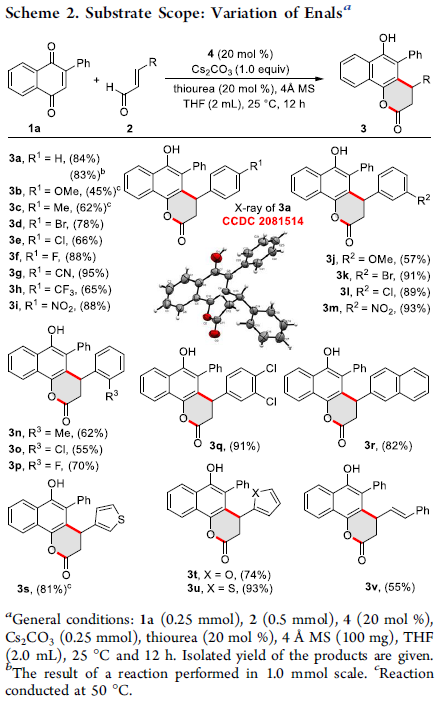
在上述最佳反应条件下,作者首先对烯醛的底物应用范围进行考察(Scheme 2)。研究表明,一系列带有供电子基与吸电子基取代的芳基烯酮底物均能较好地与上述反应条件兼容,并获得相应的产物3a–3p,收率为45-95%。其次,双取代的烯醛和β-杂芳基取代的烯醛均为合适的底物,获得产物3q–3u,收率为74-93%。此外,使用共轭的双烯醛底物时,也可获得55%收率的δ-内酯产物3v。然而,脂肪族烯醛未能顺利进行反应。
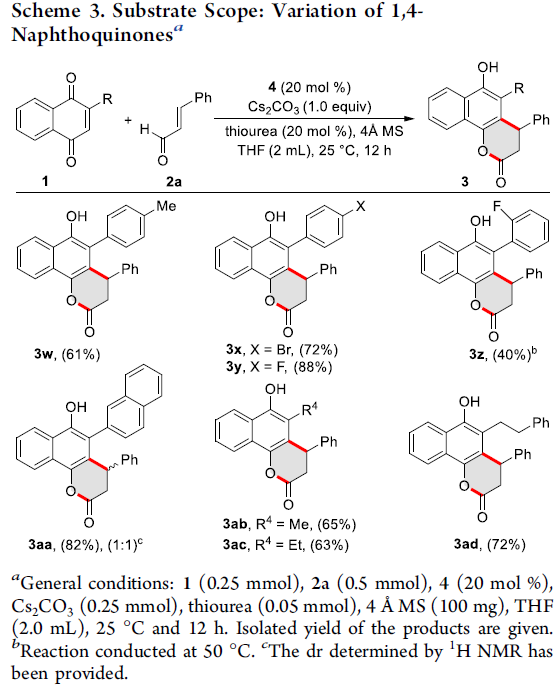
接下来,作者对2-取代1,4-萘醌底物的应用范围进行考察(Scheme 3)。研究表明,当底物中的R取代基为各种芳基取代时,均可顺利反应,获得相应的产物3w–3z,收率为40-88%。其次,当底物中的R取代基为萘基时,可获得82%的收率产物3aa,dr为1:1。此外,当底物中的R取代基为烷基时,也均为合适的底物,获得相应产物3ab–3ad,收率为63-72%。
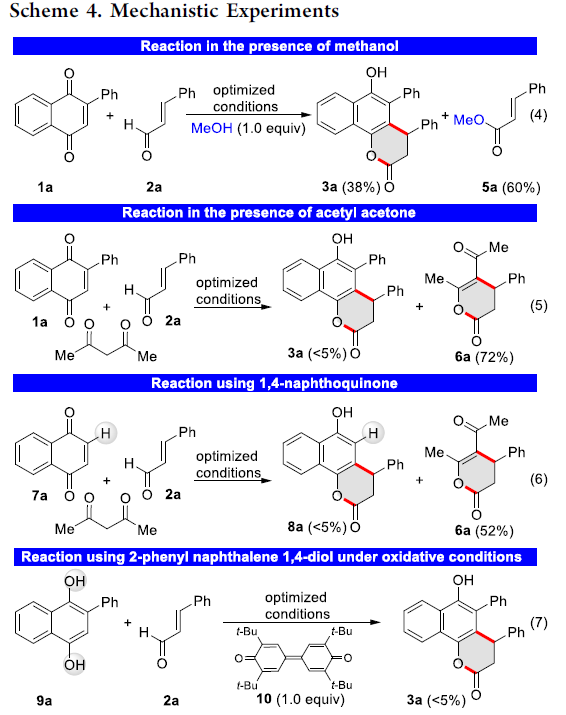
为了提出合理的反应机理,作者进行一系列相关的实验研究(Scheme 4)。首先,在1a和2a的反应体系中加入甲醇时,可获得38%收率的产物3a以及60%收率的甲酯化合物5a(eq 4)。其中,甲酯化合物5a可能是通过高烯醇负离子中间体氧化为α,β-不饱和酰基唑鎓中间体,然后与甲醇进行亲核加成而形成的。为了确认生成α,β-不饱和酰基唑鎓中间体,作者在在1a和2a的反应体系中加入乙酰丙酮,获得72%收率的二氢吡喃酮6a,并且仅观察到痕量3a的生成(eq 5)。这些实验表明,1a可作为氧化剂,用于将高烯醇负离子中间体转化为α,β-不饱和酰基唑鎓中间体。其次,当使用未取代的1,4-萘醌7a作为底物时,仅获得痕量得所需产物8a,同时以52%的收率形成6a,从而表明1,4-萘醌的C2取代对于[3+3]环化至关重要(eq 6)。
因此,作者提出了两种可能的[3+3]环化机理。第一种为涉及高烯醇负离子中间体的形成的过程(eq 3)。第二种可能性是α,β-不饱和酰基唑鎓中间体与原位形成的2-苯基萘1,4-二醇9a的[3+3]环化过程。为了验证机理的正确性,作者在9a与2a的反应体系中加入双醌氧化剂10,但未获得所需的产物3a,从而排除了α,β-不饱和酰基唑鎓参与[3+3]环化的可能性(eq 7)。
在当前条件下使用1a和2′-羟基查耳酮进行的竞争实验(分子间)表明,1a的反应速度比2′-羟基查耳酮快。1a较快的反应性可能是由于芳香性驱动的[3+3]环化过程导致。在使用1a和查耳酮进行的分子间竞争实验中观察到了类似的情况。
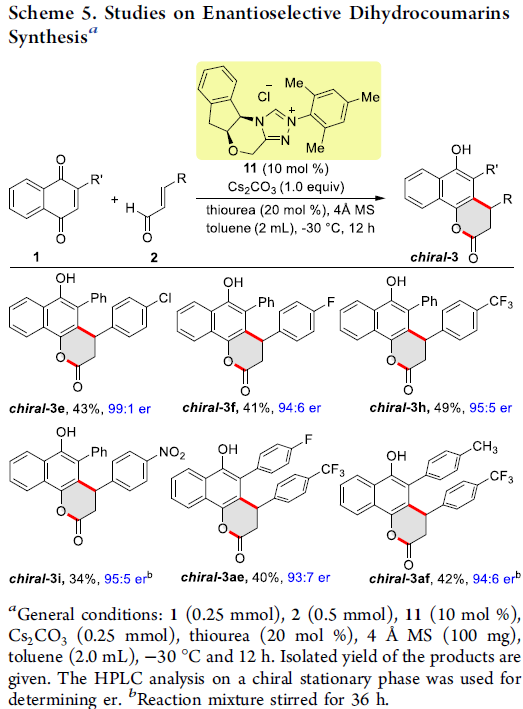
此外,作者还对反应的对映选择性版本进行了研究(Scheme 5)。当使用催化剂11时,1a可与芳基上含有4-Cl、4-F、4-CF3和4-NO2取代的肉桂醛反应,获得相应的手性产物3e–3i,收率为34-49%,er为94:6-99:1。同时,1,4-萘醌底物的2位取代为不同取代的芳基时,也可与2顺利反应,获得手性产物3ae和3af,收率为40-42%,er为93:7-94:6。
总结
Akkattu T. Biju课题组报道了一种NHC催化α,β-不饱和醛与2-取代1,4-萘醌的[3+3]环化反应,合成一系列官能团化的二氢香豆素衍生物。同时,反应涉及NHC-高烯醇负离子引发的Michael-异构化-内酯化的串联反应。机理研究表明,在[3+3]环化反应中,反应涉及NHC-高烯醇负离子中间体的形成。此外,使用手性NHCs,可获得收率高达49%和er值高达99:1的手性产物。
参考文献
[1] (a) X. Chen, H. Wang, Z. Jin, Y. R. Chi, Chin. J. Chem. 2020, 38, 1167. doi: 10.1002/cjoc.202000107(b) H. Ohmiya, ACS Catal. 2020, 10, 6862. doi: 10.1021/acscatal.0c01795
(c) T. Ishii, K. Nagao, H. Ohmiya, Chem. Sci. 2020, 11, 5630. doi: 10.1039/D0SC01538E
[2] R. J. Breslow, J. Am. Chem. Soc. 1958, 80, 3719. doi: 10.1021/ja01547a064 [3] C. Burstein, F. Glorius, Angew. Chem. Int. Ed. 2004, 43, 6205. doi: 10.1002/anie.200461572 [4] (a) S. S. Sohn, E. L. Rosen, J. W. Bode, J. Am. Chem. Soc. 2004, 126, 14370. doi: 10.1021/ja044714b(b) K. Zeitler, Angew. Chem. Int. Ed. 2005, 44, 7506. doi: 10.1002/anie.200502617
[5] J. L. Li, B. Sahoo, C. G. Daniliuc, F. Glorius, Angew. Chem. Int. Ed. 2014, 53, 10515. doi: 10.1002/anie.201405178 [6] J. Xu, S. Hu, Y. Lu, Y. Dong, W. Tang, T. Lu, D. Du, Adv. Synth. Catal. 2015, 357, 923. doi: 10.1002/adsc.201401070 [7] J. Izquierdo, A. Orue, K. A. A. Scheidt, J. Am. Chem. Soc. 2013, 135, 10634. doi: 10.1021/ja405833m [8] V. Nair, M. Poonoth, S. Vellalath, E. Suresh, R. Thirumalai, J. Org. Chem. 2006, 71, 8964. doi: 10.1021/jo0615706 [9] (a) C. Guo, M. Fleige, D. Janssen-Müller, C. G. Daniliuc, F. Glorius, Nat. Chem. 2015, 7, 842. doi: 10.1038/nchem.2337(b) J. Zhang, Y. S. Gao, B. M. Gu, W. L. Yang, B. X. Tian, W. P. Deng, ACS Catal. 2021, 11, 3810. doi: 10.1021/acscatal.1c00081
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载




















No comments yet.