作者:石油醚
导读
薄层色谱(Thin layer chromatography, TLC)是一种广泛应用于工业和化学研究的技术,尤其是有机化学领域。TLC技术因其成本低廉,操作简单等优势,在本科生化学实验以及有机合成分离方面具有很大吸引力,然而不规范的TLC技术会严重阻碍其在实验室研究中的使用。目前,TLC技术在实验和教学中常见的错误有两种,一种是使用前并没有平衡TLC显影室中的溶剂蒸汽,另外一种则是以烧杯作为TLC显影室时并使用玻璃盖。今天化学空间的小编将给大家分享正确的TLC技术,供大家学习交流。
薄层色谱(Thin layer chromatography, TLC)和纸层析(Paper chromatography)在制备色谱教学[1]、反应监测[2]、食品化学[3]和植物提取物分离分析[4]等方面具有重要的意义。在工业中方面,TLC技术在食品和化妆品中化合物的鉴定、样品纯度的测定和颜色等成分的测定方面同样占据举足轻重的地位[5]。此外,薄层色谱法也可用于生物图谱等方面来确定抗生素等天然产物的纯化方法以及快速柱层析技术的开发[6]。
TLC在上述多个方面的应用均与可重复和正确的TLC技术有关,但是错误的TLC技术在日常的实验和教学中经常出现,如在线资源[7-9]和《Journal of Chemical Education》的文章中就可发现不正确的TLC技术[10,11]。在本科生基础实验中,正确的TLC技术科提高学生实验的重复性和一致性,可极大的减少结果误差等方面的问题,并且其还有助于排出色谱问题。此外,若 TLC技术应用良好,则更易于利用极性溶剂等概念讲授的色谱实验,并且可以将不同TLC技术的评价纳入实验室的实验本身。
1.TLC技术的分离原理
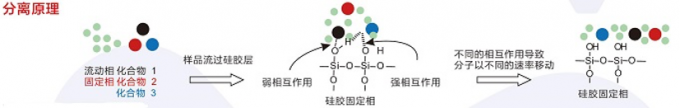
Figure 1 Simplified explanation
TLC技术依赖的是样品在固定相与流动相二者之间的相互作用:
1)样品 + 固定相 : 固定相通常是硅胶, 它的表面被 OH 基团覆盖, 化合物的氢键供体或受体越多,样品移动越慢。样品的极性越大,它移动的越慢。偶极-偶极相互作用越大,它流动就越慢。
2)样品+流动相 – 样品在流动相中的溶解度越高,移动的速度就越快。样品和流动相之间的相互作用越强,它移动得越快。
2.TLC技术的分离原理
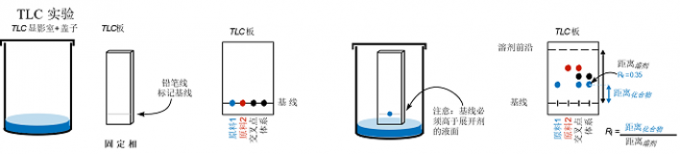
正确的TLC技术步骤(Fig.2):
1)点样:用微量进样器或毛细管进行点样。点样前,先用铅笔在层析上距末端l cm处轻轻画一横线,然后用毛细管吸取样液在横线上轻轻点样,如果要重新点样,一定要等前一次点样残余的溶剂挥发后再点样,以免点样斑点过大。一般斑点直径大于2 mm,不宜超过5 mm.底线距基线1~2.5 mm,点间距离为l mm左右,样点与玻璃边缘距离至少l mm,为防止边缘效应,可将薄层板两边刮去1-2 mm,再进行点样。
2)爬板:将点了样的薄层板放在盛在有展开剂的TLC显影室中,由于毛细管作用,展开溶剂在薄层板上缓慢前进,前进至一定距离后,取出薄层板,样品组分因移动速度不同而彼此分离。注:① TLC显影室应预先平衡蒸汽,为了加速平衡可在显影室底部垫入滤纸;②薄层板点样后,应待板上溶剂挥发完,再放入TLC显影室中展开;③TLC显影室应密闭,展距一般为8~15 cm;④展开后的薄层板用适当的方法,使板上溶剂挥发完全,然后进行检视;⑤ Rf值一般控制在0.3~0.8。
3)分析:展开后的薄层板经过干燥后,常用紫外光灯照射或用显色剂显色检出斑点(常用的显色剂见Chem-Station)。对于无色组分,在用显色剂时,显色剂喷洒要均匀,量要适度。紫外光灯的功率越大,暗室越暗,检出效果就越好。展开分离后,化合物在薄层板上的位置用比移值(Rf值)来表示。化合物斑点中心至原点的距离与溶剂前沿至原点的距离的比值就是该化合物的Rf值。
Figure 2 Running a TLC experiment
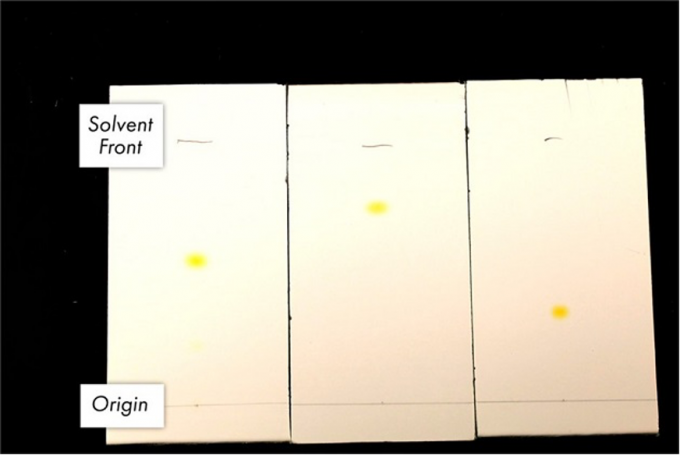
错误的TLC技术:在薄层色谱板上点样,并向烧杯中加入展开剂,随后立刻将薄层色谱板放入烧杯,再用观察玻璃覆盖烧杯。尽管错误的方法会得到一些有用的信息,但即使是同一个人在多次操作中结果与斑点移动距离是不一致(Fig.1)。该现象主要原因是溶剂充分与烧杯中的大气平衡,并且溶剂蒸汽也会从玻璃和烧杯间的缝隙溢出,从而导致TLC不具有重复性
Figure 3 TLC of dimethyl yellow. (Picture from J. Chem. Educ.)
3. TLC技术对快速柱层析的重要性
TLC技术对于快速柱层析技术的具有重要的意义,即在等梯度溶剂条件下,化合物在制备柱上的保留时间通过运行适合的TLC板,并结合式1来预测。
式1
注:Rf是保留因子,k是基于TLC板的溶剂系统下运行快速柱层析的容量因子。
容量因子是化合物在等式2所述色谱柱上保留的测量值[13]。
式2
注:此式中,t为化合物洗脱的时间,t0为柱的空隙体积,即填充溶剂的柱内的空隙,也称为“柱体积”。
假设CV = 1 + k,带入一系列的运算获得式3,式3可得洗脱化合物在TLC板中Rf和主体积有关。即若TLC板运行正确(图1中最右边的板),Rf为0.3的化合物大约需要3CV洗脱。
式3
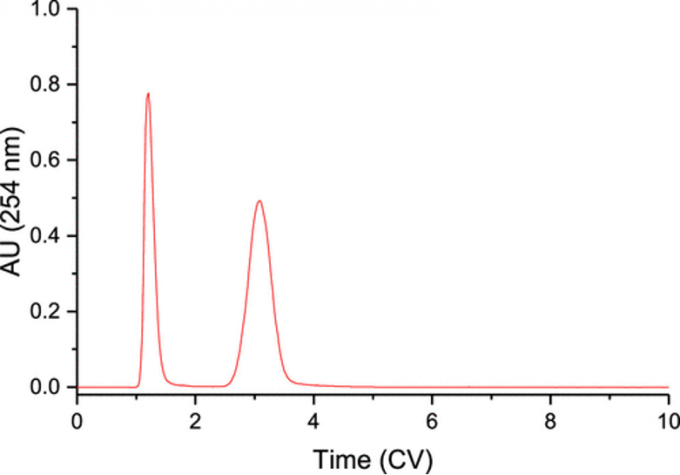
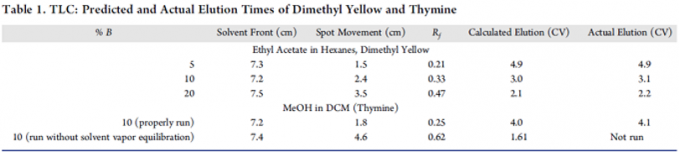
例如:Fig.4是以10%乙酸乙酯运行正确的TLC板后,以此条件运行快速柱层析色谱图。TLC板在5%乙酸乙酯中不正确运行时,柱层析的洗脱时间小于2 CV。值得注意得是,乙酸乙酯在该法中是洗脱能力较强得溶剂,进一步表明该板子运行不正确,并且混合的溶剂洗脱能力却比预期的要晚得多。其他运行TLC板的结果如Table 1所示,采用TLC和色谱法对不同溶剂组成的正己烷/乙酸乙酯体系中二甲基黄进行测定,其TLC运行正确,并获得了预期的效果。另一种化合物胸腺嘧啶是用二氯甲烷(DCM)和甲醇(MeOH)以适当的方式运行,并且没有平衡溶剂。若正确运行的TLC板的所有的情况下,计算获得洗脱和实际洗脱独有良好的一致性。相反,运行具有特定溶剂体系的二氧化硅柱将使用相同的溶剂体系产生适当运行的TLC板的Rf。对于表1中的第一次运行,t的值为4.9,t0为1 CV,其k为(4.9-1/1)= 3.9;,Rf = 1/(1+3.9) = 0.204,非常接近测量值0.21。
Table 1. TLC: Predicted and Actual Elution Times of Dimethyl Yellow and Thymine (Picture from J. Chem. Educ.)
4.结论
薄层色谱(Thin layer chromatography, TLC)和纸层析(Paper chromatography)在色谱、反应检测、实验教学、提取物的分离分析、工业等方面具有重要的意义。TLC技术因其廉价,易于操作等优势,在本科生化学实验和有机合成等方面具有重要的意义。
参考文献
- [1] M. Xie, P. Inguva, W. Chen, N. Prasetya, A. Macey, P. DiMaggio, U. Shah, C. Brechtelsbauer, J. Chem. Educ. 2020,97, 1001-1007, doi:10.1021/acs.jchemed.9b01076.
- [2] U. A. T. Brinkman, G. De Vries, J. Chem. Educ. 1972, 49, 545, doi: 10.1021/ed049p545.
- [3] H. Dickson, K. W. Kittredge, A. M. Sarquis, J. Chem. Educ. 2004, 81, 1023, doi: 10.1021/ed081p1023.
- [4] J. L. Torres y Torres, S. L. Hiley, S. P. Lorimor, J. S. Rhoad, B. D. Caldwell, G. L. Zweerink, M. Ducey, J. Chem. Educ. 2015, 92, 900-902, doi: 10.1021/ed500977r.
- [5] B. J. Sjursnes, L. Kvittingen, R. Schmid, J. Chem. Educ. 2015, 92, 193-196, doi: 10.1021/ed400519v.
- [6] Applications of Thin Layer Chromatography. https://www.milesscientific.com/applications-of-thin-layer-chromatography/
- [7] Thin Layer Chromatography and Melting Point Determination: Detection of Caffeine in Various Samples. http://course1.winona.edu/tnalli/spring05/209labs/expt3.pdf
- [8] Thin Layer Chromatography. http://www.chem.ucla.edu/~bacher/General/30BL/tips/TLC1.html
- [9] Chemistry LibreTexts. Thin Layer Chromatography. https://chem.libretexts.org/Bookshelves/Ancillary_Materials/Demos_Techniques_and_Experiments/General_Lab_Techniques/Thin_Layer_Chromatography
- [10] C. Rollins, J. Chem. Educ. 1963, 40, 32, doi: 10.1021/ed040p32.
- [11] K. D. Revell, J. Chem. Educ. 2011, 88, 1413-1415, doi: 10.1021/ed101195v.
- [12] J. J. Nash, J. A. Meyer, B. Everson, J. Chem. Educ. 2001, 78, 364, doi: 10.1021/ed078p364
- [13] D. Nurok, Chem. Rev. 1989, 89, 363-375, doi: .10.1021/cr00092a007.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载





















No comments yet.