nuo’be瑞典皇家科学院(Royal Swedish Academy of Sciences)在10月5日宣布了2016年诺贝尔化学奖(Nobel Prize in Chemistry),最终颁给了法国的Jean-Pierre Sauvage、英国的J Fraser Stoddart、荷兰的Bernard Feringa以表彰他们在分子机器上做出的贡献。
以往诺奖得主的研究一般给人应用性很广的印象,而这次着实有点出乎意料,分子机器的研究说实话完全还没有到应用的步骤。
Anyway,这一次受赏的研究属于超分子化学(有机化学)领域,按照以往的周期来看,确实也是五年一次。另外,超分子化学的得奖最早是从1987年Cram, Lehn, Pedersen三位开始的。
而这次获奖的三位大牛一直也是该领域诺奖候补的最热门人选,虽然在诺贝尔奖化学家候补名单Chem-Station2016版中只出现了Stoddart,但是其他两位的业绩也都是引人瞩目的。接下来,小编想为大家具体介绍下这三人的工作。
分子机器的重要一部分:轮烷与索烃
对分子机器的研究发展起着至关重要的作用的是被称为mechanically-interlocked molecule的物质群。其中的代表就是轮烷与索烃。
索烃(catenane)、是环状化合物像锁一样圈在一起连接成的结构,名字取于希腊语中的catena。而另一方面轮烷(rotaxane)是轮状结构被一根棒状的「轴」贯穿形成的挂何物,名字来自于拉丁语中的轮(rota)与轴(axis)。
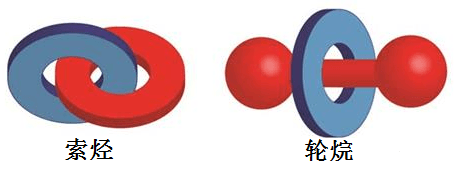
索烃的两个圈以及轮烷的圈与轴之间并没有共价键结合固定,所以相互之间是相对可以移动的。索烃一般只要圈圈不断裂,是能够稳定存在的,轮烷的话圈在轴上是可移动的。为了使得轮烷能够稳定存在(圈不脱离轴),一般来说轴的两端是比较大的构型,作为一个塞子防止圈脱离轴。
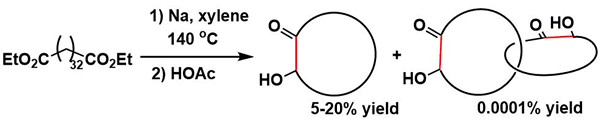
索烃的世界首次合成是由贝尔实验室的Harry Wasserman在1960年成功实现的。该合成策略很简单,就是以两端带由于酯基的超长链烃为原料进行Acyloin Condensation。但是单单是长链底物的自身环化产率就很低,而两分子串联的过程也十分偶然,最终以极低的产率0.0001%得到了世界第一个索烃。为了得到足够量的产物,据说该反应是在浴缸中进行的。。。可见底物的量是多么巨大,以当时的技术合成索烃是多么不容易。而其实从那开始到高效合索烃也经历了很多年的探索。
轮烷・索烃的高效合成!:Jean-Pierre Sauvage
实现Mechanically-interlocked molecule的合成breakthough的就是这次获奖者中的Jean-Pierre Sauvage教授。
Jean-Pierre Sauvage教授巧妙了利用通过金属离子(铜)的配位能进行的模板合成的手法,成功开发了索烃的高效率合成法。(1983年)。该手法的缩略图如下所示。1价铜可以配位成正四面体的配位结构,利用这个关键性要素,巧妙的使得索烃的两个圈圈串联在一起。
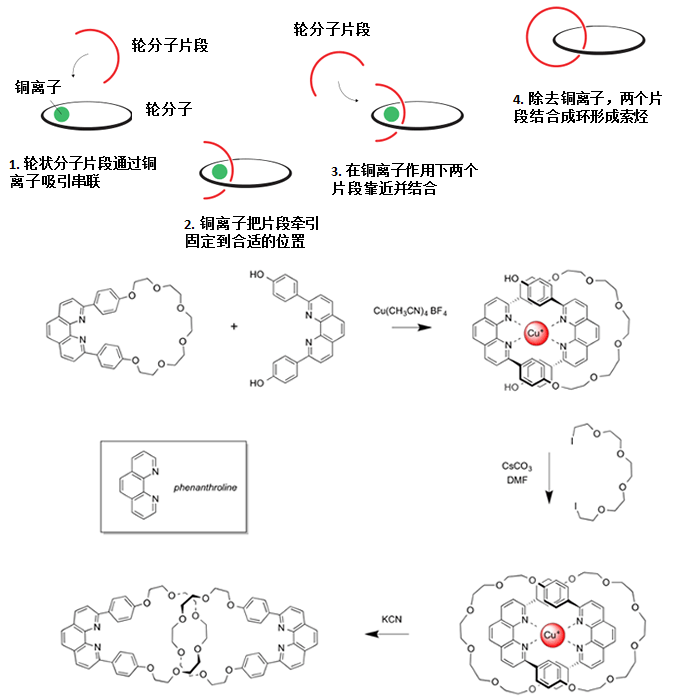
这种合成手法的实用性特别广,利用相同的原理可以合成各种不同拓扑的化合物。其中小编在下图中给出了几个比较有代表性的例子。真可以说。。其实合成也是门艺术。
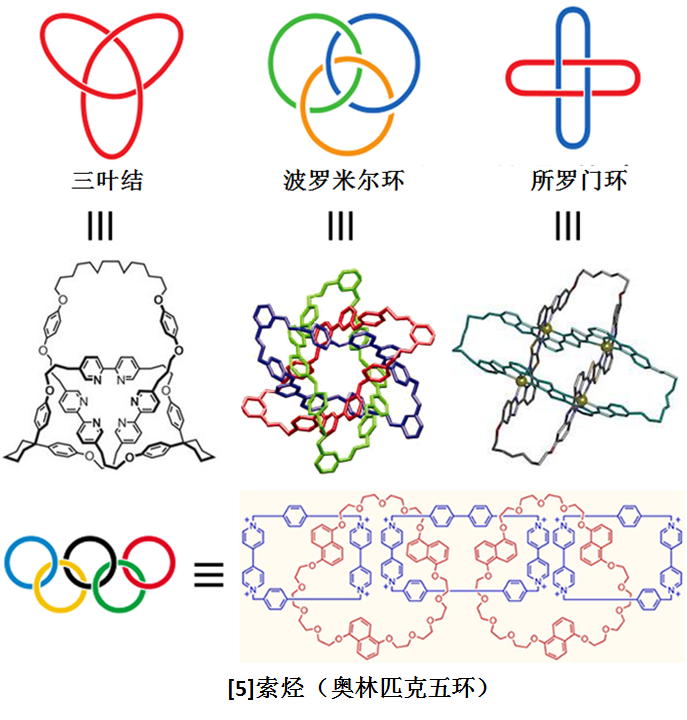
另一方面,作为合成化学家来说,通常都必须考虑合成的化合物的用途。仅仅依靠个人的兴趣,以一种玩耍的态度进行研究的话,当然小编个人认为也是非常OK的,但是往往会遭人诟病,也很难申请经费继续研究。而对于这些超分子来说,其中的实用性也确实在一开始是一大难题。
但是从“颜值”来看,作为一直从事小分子合成研究的小编来看,真的是不得不承认这些分子「长得非常漂亮!」。突然也意识到,其实不能局限于自己的小分子合成中,应该多关注下有机化学甚至生物材料那些交叉领域,从而让自己的视野变的更广阔。
轮烷分子开关合成!:J Fraser Stoddart
J Fraser Stoddart教授在Jean-Pierre Sauvage教授的合成法上得到灵感,创制合成了具有「bistable」性质的索烃・轮烷化合物。该分子具有两种状态,而该两种状态在外部刺激的状态下可以人工的进行转换,所以有望用作分子开关。Stoddart教授在1989年合成了这样的轮烷分子,并在1991年给出了可以用于分子开关的可能性展示。下图中的分子是其中的一个实例,该分子在氧化还原或者pH变化条件下,通过正离子电荷的作用来进行该分子的两种状态的转换。在产生正电荷时候,由于左侧的苯二胺结构与轮上的正电荷有个排斥作用,所以轮环的位置就保持在右侧对苯二酚那块。而当正电荷消失时候,由于π-π相互作用占决定性优势,轮环就停留在左侧的苯二胺侧。
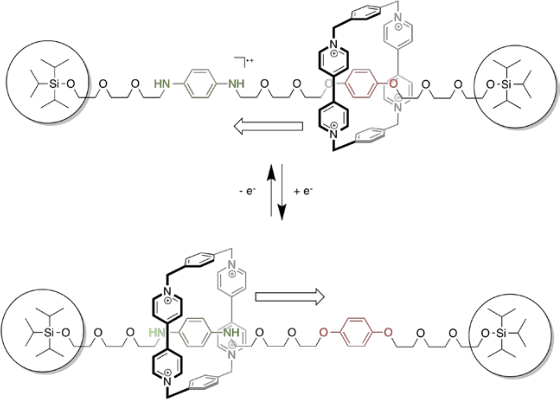
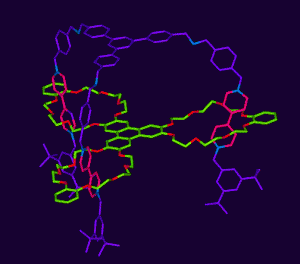
Stoddart教授逐步把这个设计理念发展扩大,目前为止合成除了可以控制更多复杂的动作的化合物,并且成功应用到了功能性材料上。例如在2004年,在拥有三个”脚手架”的金属表面上,合成出了底座可以升降的[分子电梯](下图所示绿色分子可以上下移动)。另外Stoddart组还在进行具有变形能力的分子肌肉、通过分子层级的氧化还原进行信息记录的超高密度分子记忆存储等的开发。
分子电梯
分子肌肉与超高密度分子记忆存储的应用
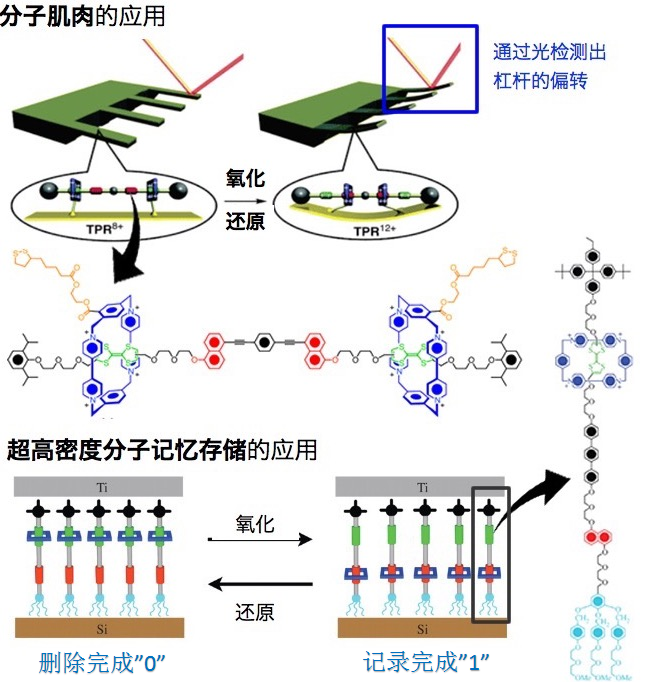
由于这些超分子的合成费用消耗比较高,说实话目前为止还没有能够实现实用化,从视觉感官上很容易理解,也确实是非常有趣的科学。
合成分子马达!:Bernard Feringa
不同于上述的利用轮烷・索烃作为分子开关的研究,Feringa教授利用完全不同的机械分子机制合成了分子马达。
详细的来说,Feringa教授的代表作是世界首次合成了利用光照射驱动的单一方向旋转的光驱动型分子马达(1999年)。最初期合成的是立体位阻比较大的轴手性分子。这种带有双键轴的化合物在紫外线的照射下,双键的一部分断裂,并且以此为轴开始旋转。这种性质在很早以前就已经被广为所知。但是Feringa教授利用这种性质进一步巧妙地设计了新的分子,使得该分子只能朝着单一方向旋转(下图所示)。旋转的能量来自于光或者热,而旋转方向由手性碳的手性环境决定。通过对分子结构的最优化后,该分子可以以相当高的速度旋转(室温下,MHz order),是一个非常有发展前景的分子马达。
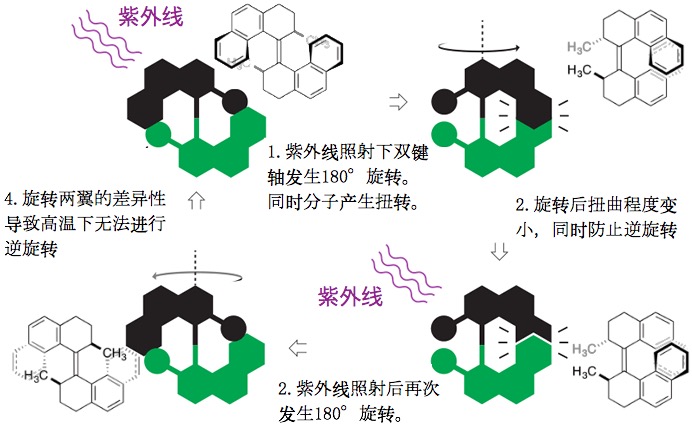
Fearing教授把该分子马达产生的旋转力运用到了宏观情况。下图所示分子1在液晶薄膜上排列,在光照下,其产生的旋转力可以使得薄膜上放置的物体(毫米长)朝一个方向旋转。也就是说,实现了对数万倍以上物体的力的传输,确实是一项十分巧妙有趣的设计。
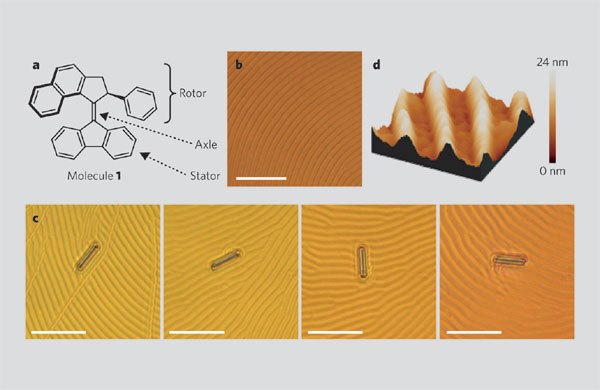
另一方面,还设计出了搭载有”轮胎”的分子马达,被称作「纳米四轮驱动」。利用电能使得分子马达朝一个方向旋转,可以使得分子在金属表面上“跑”。该“跑动”通过显微镜得到了确认。
结语
这次诺奖的研究与以往注重实用性不同,是趣味性很强的研究,实在是完全出乎了小编的意料,不知道大家是否有预测到呢?但是另一方面这也是值得令人振奋的,他们的研究在分子的层面上唤起了科研人员的童心。创造出这么多有意思的,颜值很高的分子也会让人心情愉悦。
相比于目前过于强调使用性的主流来说,回归科研本身,从事一些十分有创造性的研究也不失为一股清流。最后再次祝贺三位获奖教授!同时期待我国能早日出现第二个自然科学的诺奖!
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!






















No comments yet.